
【题目】下列实验操作错误的是( )
A.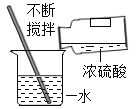 稀释浓硫酸B.
稀释浓硫酸B.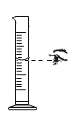 液体的量取
液体的量取
C.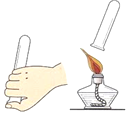 检验氢气的纯度D.
检验氢气的纯度D.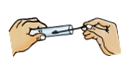 往试管里送入固体粉末
往试管里送入固体粉末
【答案】B
【解析】
A、浓硫酸稀释时,一定要浓硫酸沿器壁慢慢注入水里,并不断用玻璃棒搅拌,故A操作正确,不符合题意;
B、读数时,视线要跟量筒内液体的凹液面的最低处保持水平,再读出液体体积,图中视线未与凹液面最低处持平,故B操作错误,符合题意;
C、检验氢气纯度的方法:用排水法收集一试管氢气,用拇指堵住试管口,管口向下移近酒精灯火焰,松开拇指点火,如果听到尖锐的爆鸣声,表明氢气不纯,需要再收集,再检验,直到听到很小的响声,才表明氢气已经纯净,故C操作正确,不符合题意;
D、粉末状药品的取用方法:先将试管倾斜,把盛药品的药匙(或者纸槽)小心地送入试管底部,再使试管直立起来,故D操作正确,不符合题意。
故选B。


 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:初中化学 来源: 题型:
【题目】某校化学社团—“拉瓦锡实验室”的活动丰富多彩。他们在实验室废液桶中收集了含有大量FeSO4、CuSO4的废水,为防止废水直接排放到下水道造成重金属污染和浪费,设计了如图所示
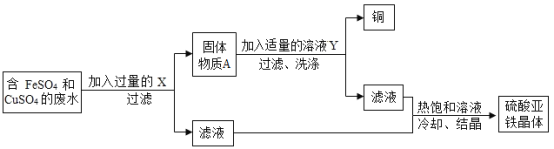
(1)整个实验过程中多次采用过滤,该操作用到的玻璃仪器有烧杯、________和玻璃棒。
(2)所加物质X是________________________(填名称),其加入废水后发生反应的化学方程式为____________________________________。溶液Y是____________(填名称);固体A中含有的物质是____________(填化学式)。
(3)该小组的同学又收集到一些含硝酸银、硝酸铜的混合废液,同学们向其中加入一定量锌粉,反应停止后过滤,滤液仍为蓝色。则下列有关判断正确的是____________(填字母)。
A 滤渣中一定有银,没有铜和锌
B 滤渣中一定有银和锌,可能有铜
C 滤液中一定有硝酸锌、硝酸铜、硝酸银
D 滤液中一定有硝酸锌、硝酸铜,可能有硝酸银
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙两种物质的溶解度曲线如图所示。下列说法不正确的是( )
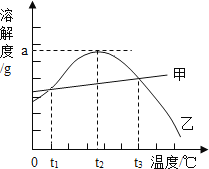
A.在t1℃、t3℃时甲、乙两物质的溶解度相等
B.在t1℃至t3℃之间,乙的溶解度大于甲的溶解度
C.将甲、乙的饱和溶液从t3℃降到t1℃,析出甲、乙的质量相等
D.将t2℃时接近饱和的乙溶液变为饱和溶液可采取升温或降温的方法
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某地成功处置了一辆满载三氯化磷( PC13)的车辆泄漏事故。三氯化磷是一种重要的无机工业产品,无色液体、密度1.574g/cm3(21℃),熔点-112℃,沸点75.5℃,易燃。遇水反应生成亚磷酸(H3PO3)和氯化氢,与有机物接触会着火。下列说法错误的是( )
A.H3PO3中磷元素的化合价为+3
B.运输途中应防雨淋和防高温
C.运输过程中如果发生燃烧时,可以用水浇灭
D.三氯化磷与水反应的化学方程式: ![]()
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列设计方案可行,化学方程式书写及其反应类型都正确的是
A.清洗试管壁上附着的铜: Cu+H2SO4=CuSO4+H2↑ 置换反应
B.测定空气中氧气的含量: P+O2![]() P2O5 化合反应
P2O5 化合反应
C.湿法冶铜: Fe+CuSO4═FeSO4+Cu 置换反应
D.实验室制取二氧化碳: CaCO3![]() CaO+CO2↑ 分解反应
CaO+CO2↑ 分解反应
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在一定条件下,A和B能发生化学反应生成C和D,其微观示意图如下所示:

请回答下列问题:
(1)上述反应过程中,属于氧化物的是①______(填字母),从微观的角度说明你判断的依据是②_______________。
(2)该反应的的化学方程式为________。属于________反应(填基本反应类型)
(3)画出比一个B分子少一个电子原子结构示意图:_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】能源是人类生存和发展的基础,能源成为人们日益关注的问题。
①化石燃料包括煤、___________、天然气等,是重要
的能源;目前正在利用和开发的新能源有核能、生物质能、___________ ___________ (填一种)等
②发射卫星的火箭可使用液氢作燃料,液氢在液氧中燃烧的化学方程式为:
_________________________________,该反应属于基本反应类型中的______________________ 反应
③物质R是一种可再生绿色能源,其燃烧的化学方程式为 R+3O2 ![]() 2CO2+3H2O,则R的化学式为________________________________
2CO2+3H2O,则R的化学式为________________________________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验窒常会产生含硫酸的废水,需经处理至中性.某兴趣小组同学配制一定质量分数的氢氧化钾溶液来处理酸性废水。
(l)定性检测废水,检测废水呈酸性的方法是_______________________。
(2)配制200g质量分数为5.6%的氢氧化钾溶液
①计算m(KOH)=__________g,V(H2O)=______mL(水的密度近似为1.0gmL﹣1)。
②称取氢氧化钾
调节托盘天平平衡后,将一只烧杯放在托盘天平的左盘,称量其质量。然后_____(按操作先后顺序,填字母),直至天平平衡。
a.向烧杯中加氢氧化钾固体 b.按需要添加砝码、移动游码
(3)定量测定废水
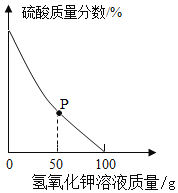
取酸性废水样品100g,逐滴加入5.6%的氢氧化钾溶液,废水中硫酸的质量分数变化如图所示.(假设废水中其他成分不与氢氧化钾反应且不含硫酸钾)
①P点对应溶液中一定存在的阳离子有____(填离子符号)。
②酸性废水中硫酸的质量分数为________(用百分数表示,保留到0.1%)。
③计算当废水处理至中性时,溶液中硫酸钾的质量分数(写出计算过程,结果用百分数表示,保留到0.l%)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】一种用软锰矿(主要成分是MnO2)制备KMnO4的工艺中主要涉及下列反应:
①2MnO2+O2+ 4KOH![]() 2K2MnO4+ 2H2O
2K2MnO4+ 2H2O
②2K2MnO4+2H2O==2KMnO4+2KOH+H2↑
下列有关说法正确的是
A. K2MnO4中锰元素显+7价 B. KMnO4属于盐类物质
C. 反应②属于复分解反应 D. 该制法中K2MnO4是主要原料
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com