

| ||
| ||


科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
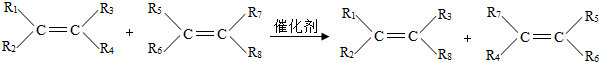
| A、置换反应 | B、分解反应 |
| C、化合反应 | D、复分解反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
 已知A、B、C、D、E是初中化学常见的物质,D物质的水溶液为蓝色,E是相对分子质量最小的氧化物,它们的转化关系如图所示:
已知A、B、C、D、E是初中化学常见的物质,D物质的水溶液为蓝色,E是相对分子质量最小的氧化物,它们的转化关系如图所示:查看答案和解析>>
科目:初中化学 来源: 题型:
 如图是某胃药标签上的部分内容,某中学化学兴趣小组欲测定该药品中碳酸氢钠(NaHCO3)的质量分数,取10片该药品研碎放入烧杯中,再向烧杯中滴加稀盐酸至恰好完全反应(杂质不溶于水,也不参加反应.反应的化学方程式为
如图是某胃药标签上的部分内容,某中学化学兴趣小组欲测定该药品中碳酸氢钠(NaHCO3)的质量分数,取10片该药品研碎放入烧杯中,再向烧杯中滴加稀盐酸至恰好完全反应(杂质不溶于水,也不参加反应.反应的化学方程式为查看答案和解析>>
科目:初中化学 来源: 题型:
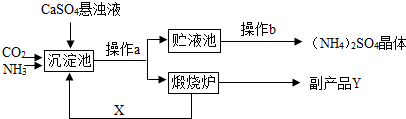
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com