
【题目】如图所示为实验室中常见气体制备、净化、干燥、收集和进行实验探究的部分仪器(组装实验装置时,可重复选择仪器),某化学小组的同学欲利用其进行下列各实验,回答下列问题:
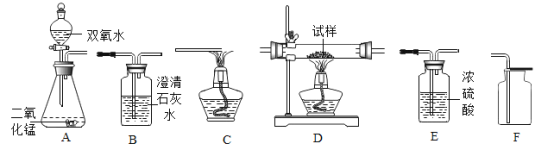
(1)该组欲在实验室中制备并收集干燥的氧气。
①所选仪器的连接顺序为____________(填写仪器序号字母)。
②制取氧气所发生反应的化学方程式为____________________________________。
③氧气在空气中有相对稳定的含量是由于在自然界中存在氧的循环,请写出自然界中消耗氧气的一条途径______________________。
(2)用干燥纯净的氧气对纤维素的组成进行分析探究实验(资料显示纤维素只含C、H、O三种元素)。所选装置按“氧气→D→E→B→碱石灰干燥管”的顺序连接(实验前检查装置的气密性,假设所发生的化学反应都完全充分进行)。装置B中出现的现象为___________,装置D的玻璃管中放入纤维素试样的质量为1.62g,充分反应后,测得装置E的质量增加0.9g,装置B的质量增加2.64g,通过计算可得出纤维素中C、H、O三种元素的质量比为___:___:_____(计算结果用最简整数比表示)。
【答案】AEF 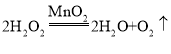 呼吸作用 澄清石灰水变浑浊 36 5 40
呼吸作用 澄清石灰水变浑浊 36 5 40
【解析】
过氧化氢在二氧化锰催化作用下分解生成水和氧气,氧气密度比空气大,可以用向上排空气法收集;
浓硫酸具有吸水性,可作氧气的干燥剂;
光合作用生成氧气,呼吸作用消耗氧气;
化学反应遵循质量守恒定律,即反应前后元素种类、原子种类及个数和质量都不变。
(1)
①所选仪器的连接顺序为:通过A制取氧气,通过E干燥氧气,通过F收集氧气。
故填:AEF。
②过氧化氢在二氧化锰催化作用下分解生成水和氧气,反应的化学方程式为: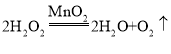 。
。
③自然界中消耗氧气的一条途径是呼吸作用,呼吸作用过程中消耗氧气,生成二氧化碳等物质。
故填:呼吸作用。
(2)纤维素与氧气在加热时反应生成二氧化碳和水,通过E浓硫酸干燥后进入装置B,B中澄清石灰水遇到二氧化碳要变浑浊;
测得装置E的质量增加0.9g,说明生成了0.9g水,装置B的质量增加2.64g,说明生成了2.64g二氧化碳;
0.9g水中氢元素质量为:![]() ;
;
2.64g二氧化碳中碳元素质量为:2.64g×![]() =0.72g;
=0.72g;
水中的氢元素、二氧化碳中的碳元素都来自于纤维素,故纤维素中碳元素质量是0.72g,氢元素质量是0.1g,纤维素只有三种元素,所以其中氧元素质量就等于纤维素质量减去氢和碳元素的质量,即:1.62g-0.72g-0.1=0.8g,
纤维素中C、H、O三种元素的质量比为:0.72g:0.1g:0.8g=36:5:40,
故填:36;5;40。


科目:初中化学 来源: 题型:
【题目】不少同学都被蚊虫叮咬过,感觉又痛又痒。同学们从化学课上知道:蚊虫叮咬时能在人的皮肤内分泌出蚁酸刺激皮肤。课外兴趣小组同学决定对蚁酸进行探究。
(提出问题)蚁酸的成分是什么?它有什么性质?
(查阅资料)蚁酸是一种有机酸,化学名称叫做甲酸,化学式为HCOOH;蚁酸在一定条件下会分解生成两种氧化物。
(实验探究一)探究蚁酸的酸性。
(1)向盛有蚁酸溶液的试管中滴加紫色石蕊试液,观察到溶液颜色变成红色,说明蚁酸溶液显_____;
(2)将锌粒放入盛有蚁酸溶液的试管中,有气泡产生,该气体是________。
(实验探究二)探究蚁酸分解的两种产物。
(1)小芳同学根据蚁酸中含有____________元素,推测出生成物中含有水;
(2)另一种生成物是气体,小敏提出两种猜想: 猜想①:该气体是CO2 ;猜想②:该气体是____;他们将蚁酸分解产生的气体通过如图装置(铁架台已略去),观察现象。
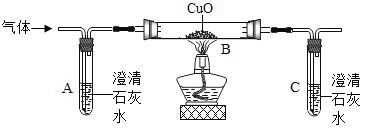
Ⅰ.实验时装置A中无明显变化,则猜想①__________(填“成立”或“不成立”);
Ⅱ.装置B中的现象是_________,装置C中发生反应的化学方程式为___________________。
(讨论交流)从环保角度看,该装置的缺陷是____________,处理的方法是_________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某干燥剂含有CaO、NaOH和CaCl2中的两种物质。为了探究其成分,设计了如图所示实验。下列说法正确的是( )
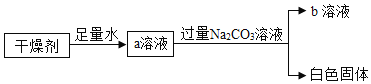
A.溶液a形成过程中一定只发生物理变化B.b溶液中一定有NaOH和Na2CO3
C.得到的白色固体一定不是纯净物D.干燥剂一定由 NaOH和CaCl2组成
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学小组为探究铝、铜、银三种金属的活动性顺序,设计了下图所示实验方案(金属 丝使用时均已用砂纸打磨)。下列说法正确的是()
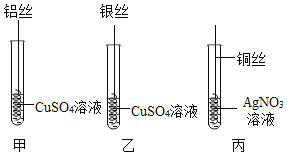
A.由实验甲可知金属活动性:Al>Cu
B.由实验乙可知金属活动性:Ag>Cu
C.实验甲中的CuSO4改为CuCl2,也能完成本实验探究
D.若要探究铝、铜、银活动性顺序,甲、乙、丙实验必须全做
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】硫酸亚铁铵((NH4)2SO4·FeSO4·6H2O)俗称摩尔盐,可用于净水和治疗缺铁性贫血。工业上常利用机械加工行业产生的废铁屑(含有少量杂质 Fe2O3)为原料制备(如图)。
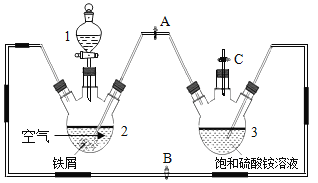
某化学兴趣小组拟用下列方案制备硫酸亚铁铵并进行相关探究。 查阅资料:
(1)FeSO4易被氧气氧化为Fe2(SO4)3,影响硫酸亚铁铵的等级。
(2)在FeSO4溶液中加入(NH4)2SO4固体可制备硫酸亚铁铵晶体,该晶体比一般亚铁盐稳定,不易被氧化,易溶于水,不溶于乙醇。
(3)在0~60℃时,硫酸亚铁铵的溶解度比硫酸铵、硫酸亚铁的溶解度小,冷却混合液至室温便析出硫酸亚铁铵。
(探究一)用如上图所示装置制备硫酸亚铁铵。实验步骤如下:
①制备 FeSO4溶液:先关闭止水夹 A,再打开止水夹 B和 C,从分液漏斗滴加稀硫酸至三颈烧瓶2中,此装置中发生的化学反应主要有(用化学方程式表示)______、_______和![]() 。该过程中氢气的作用是______。
。该过程中氢气的作用是______。
②待装置中的铁屑快反应完时,关闭止水夹_______,打开止水夹_______,观察到的现象是_______。实验时为防止三颈烧瓶2中剩余铁屑通过导管进入三颈烧瓶3中,可采取的措施 是_______。
③放置一段时间,试剂瓶底部将结晶出硫酸亚铁铵晶体,从中获得硫酸亚铁铵晶体的主要实验操作为过滤、洗涤、干燥。为洗涤(NH4)2SO4·FeSO4·6H2O 粗产品,下列方法中最合适的是______。
A 用冷水洗 B 先用冷水洗,后用无水乙醇洗
C 用 30%的乙醇溶液洗 D 用 90%的乙醇溶液洗
(探究二)探究硫酸亚铁铵样品的纯度取5g硫酸亚铁铵晶体溶于50mL水配成溶液,等分成两份,分别进行实验。
方案一:![]()
(1)实验中加入过量BaCl2溶液的目的______。
(2)利用方案一测得的数据,计算该硫酸亚铁铵样品的纯度(列出具体计算步骤)。((NH4)2SO4·FeSO4·6H2O的相对分子质量:392)__________
方案二:如图所示,向另一份中加入过量的NaOH溶液,充分反应后得到NH3
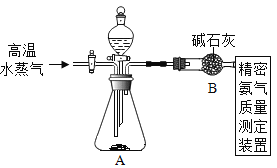
(3)(NH4)2SO4与NaOH反应的化学方程式为_______。
(4)实验中需不断通入高温水蒸气,其作用是_______。
(5)在实际测量中,利用方案二测得的样品纯度总是低于方案一测得的数值,可能的原因是______。
(探究三)对硫酸亚铁铵((NH4)2SO4·FeSO4·6H2O)晶体进行热重分析,温度与TG%的关系如下图所示
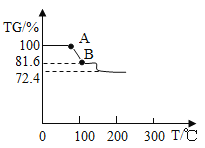
已知:温度低于 200℃,只有结晶水失去。
已知:TG% =![]()
TG%从 100%降低为 72.4%时,发生反应的化学方程式是_______ 。试计算AB段物质的化学式______________ 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列图像中有关量的变化趋势与对应叙述关系正确的是
A.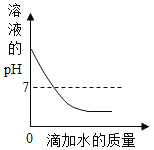 向一定量稀盐酸中加水稀释
向一定量稀盐酸中加水稀释
B.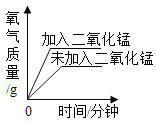 用等质量、等浓度的双氧水分别制取氧气
用等质量、等浓度的双氧水分别制取氧气
C.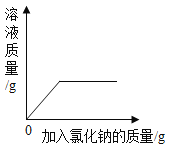 一定温度下,不饱和氯化钠溶液中加入氯化钠
一定温度下,不饱和氯化钠溶液中加入氯化钠
D.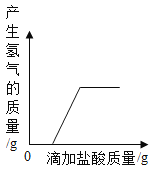 向一定质量的表面生锈的铁片中滴加盐酸至过量
向一定质量的表面生锈的铁片中滴加盐酸至过量
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某合金由铜与锌组成。现欲测定其组成,进行如下实验:取该合金样品30g放入烧杯中,然后将200g溶质质量分数为19.6%的稀硫酸平均分四份依次加入该烧杯中,每次均充分反应。实验数据如下:
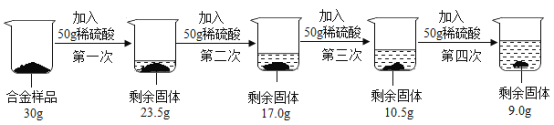
请计算:
(1)该合金中铜的质量为______________________g。
(2)第三次加入稀硫酸充分反应后,所得溶液中溶质的质量分数__________________(写出简明计算过程,结果保留一位小数)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验时,有同学不小心放错了胶头滴管,使得NaNO3溶液的试剂瓶中可能混入NaCl、NaOH、Na2CO3和 Na2SO4中的一种或几种。为了验证,他进行了如图所示的实验。
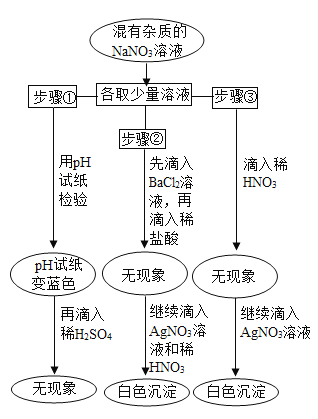
请回答:
(1)由步骤①得知,此溶液中含有(写化学式,下同)_____。
(2)由步骤②得知,此溶液中不存在_____。
(3)由步骤③得知,此溶液中含有_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】安全和合理膳食舌尖上的美味,才能使我们的身体更健康。
(1)锌、铁、钙、硒等是人体不可缺少的元素,它们都属于_____(填营养素名称);如果人体缺少铁元素可能引起的疾病是_____。
(2)如果你的午餐有:①大米饭,②水煮浑江鲤鱼,③凉拌酸辣土豆丝,其中富含糖类的是_____(填序号)。
(3)近几年,食品药品监督管理局加大对米面粮油、乳制品、肉制品、酒类、水产品等热销食品和节令食品生产企业及小作坊的日常检查和专项抽检力度。其中下列属于安全食品的是_____(填字母)。
A 用甲醛保存的海鲜类食品
B 用处理后的“地沟油”烹调的食品
C 将霉变的花生洗净蒸煮后做的拌菜
D 适量添加钙元素制成的强化食品高钙豆奶粉
(4)幼儿及青少年缺钙会患佝偻病和发育不良。下图为钙元素在元素周期表中的一些信息和另一些元素的粒子结构示意图,根据图示回答下列问题:
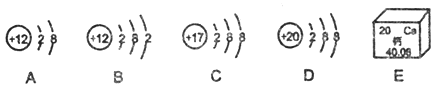
上图A、B、C、D中,具有稳定结构的粒子是_____(填字母),E图示中,“20”表示_____。某同学根据图示判断:“A、B是同一种元素,具有相似的化学性质”,你认为他的判断是否正确?_____(填“正确”或“不正确”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com