
【题目】实验室有一瓶失去标签的NaOH溶液。为测定溶液中NaOH的质量分数,取m2gNaOH 溶液于量热器中,加入m1g质量分数为10.0%的盐酸,进行若干次实验(实验中始终保持m1+m2=50g),测量并记录每次实验溶液均匀混合后的最高温度,实验结果如图所示,下列有关本实验的说法中错误的是
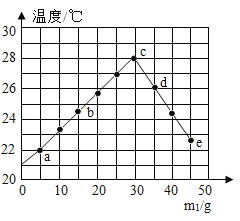
A.由图像可知,图中c点表示盐酸与氢氧化钠恰好完全反应
B.根据图像所提供的数据计算可知,溶液中NaOH的质量分数约为16.4%
C.d、e点温度比c点低,是因为反应结束温度逐渐降低
D.b点对应的溶液中含有钠离子、氯离子、氢氧根离子和水分子
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:
【题目】溶液与人们的生活息息相关。
(1)不同物质在水中的溶解能力不同,下列物质属于难溶性盐的是____(写化学式,下同);属于可溶性碱的是______,属于可溶性盐的_____。
①氢氧化钾
②硫酸钡
③氢氧化铁
④氯化银
⑤硝酸镁
(2)在盛有水的烧杯中加入以下某种物质,形成溶液过程中,温度降低。这种物质是____(填字母)
A 氢氧化钠
B 硝酸铵
C 氯化钠
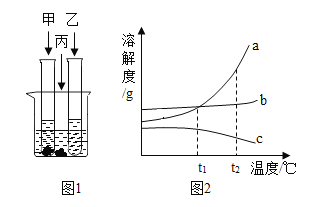
(3)室温下,将甲、乙、丙三种固体分别充分溶于两支试管和一个烧杯的水中,现象如图1所示,甲、丙固体有剩余,乙固体全部溶解。升温到 80℃时,发现甲固体全部溶解,乙固体析出,丙固体没有明显变化。
①室温下,______(选填“甲”、“乙”、“丙”)溶液一定是饱和溶液。
②图2中能表示乙物质的溶解度曲线的是_____(填“a”、“b”或“c”)。
③t1℃时,甲、丙两物质饱和溶液中溶质质量分数:甲____丙(填“>”、“<”或“=”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲物质的溶液可用作化肥、电镀液等。甲的溶解度曲线如图所示,下列说法正确的是

A.甲的溶解度是102.5g
B.甲的溶解度随温度的升高而增大
C.20℃时,100 g甲的饱和溶液中溶质质量为28.6 g
D.将70℃甲的饱和溶液升高温度或降低温度,都有晶体析出
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图所示是实验室常用的一些仪器,回答图后面的问题。
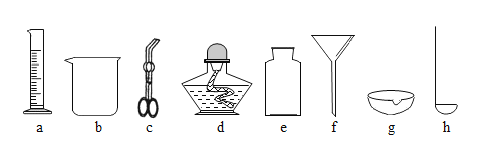
(1)根据以下实验要求,选择图中合适仪器,将编号填在相应的横线上。
①给体积约为90 mL的硝酸钾溶液加热:________;
②用固体氯化钠配制一定溶质质量分数的氯化钠溶液:__________;
③过滤粗盐水:________。
(2)除了图中的仪器,(1)中的②、③两个实验都还要用到的一种仪器是(填仪器名称)________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】以MnO2为原料制备MnSO4H2O的工业流程如图。
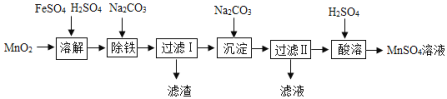
已知:①沉淀时的化学方程式为7MnSO4+7Na2CO3+11H2O=MnCO36Mn(OH)25H2O↓+7Na2SO4+6CO2↑
②MnSO4H2O和MnSO45H2O易溶于水,难溶于乙醇。
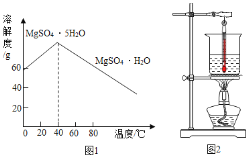
③MnSO4的溶解度曲线如图1所示。
(1)溶解时,为控制80℃,在实验室可用水浴加热如图2.水浴加热需要的玻璃仪器有酒精灯、① _____、_____。水浴加热的优点有②_____________。能加快溶解的方法有③_________(写一种)。
(2)除铁时需要搅拌,搅拌的作用是____________。
(3)过滤I所得滤液的溶质主要是Na2SO4和____________。
(4)酸溶时,MnCO36Mn(OH)25H2O与足量稀硫酸反应的化学方程式为___________________。
(5)请补充完整由流程中“酸溶”所得MnSO4溶液制备MnSO4H2O的实验方案:将MnSO4溶液转移至蒸发皿中,___________,在高于40℃时趁热过滤,____________,100℃烘干得MnSO4H2O。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列叙述及对应的化学方程式和所属基本反应类型都正确的是( )
A. 服用含氢氧化铝的药物治疗胃酸过多 2Al(OH)3+6HCl=2AlCl3+6H2O 复分解反应
B. 拉瓦锡研究空气成分 2HgO![]() 2Hg+O2↑ 分解反应
2Hg+O2↑ 分解反应
C. 用天然气作燃料 CH4+2O2![]() CO2+2H2O 氧化反应
CO2+2H2O 氧化反应
D. 验证铁的活动性比银强: Fe+2AgCl==2Ag+FeCl2 置换反应
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣小组同学在学习中和反应后,做了如下实验:
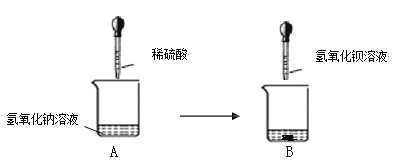
【观察与讨论】甲同学观察到 B 烧杯中出现___________ 现象,于是甲同学认为氢氧化钠和稀硫酸发生了反应。乙同学不同意甲同学的观点,其理由是________;
为了科学处理废液,同学们对 B 烧杯中上层溶液里的溶质成分进行了探究。
【提出问题】B 烧杯中溶液里的溶质含有什么物质?
【猜想与假设】甲同学猜想:Na2SO4
乙同学猜想:Na2SO4、NaOH
丙同学猜想:NaOH 、Ba(OH) 2
丁同学猜想:Na2SO4、H2SO4
【实验探究】甲同学实验:取 B 烧杯中溶液少许于试管中,向其中先滴加几滴无色酚酞试 液,溶液变成红色,然后再加入足量的稀硫酸,观察到____________________现象,于是甲同学认为乙同学猜想正确。请你评价甲同学的实验及结论_____________________;
乙同学实验:取 B 烧杯中溶液少许于试管中,向其中滴加硝酸钡溶液,观察到有白色沉淀生成,乙同学结合甲同学实验确定了溶液中溶质为 ___________填化学式);
同学们根据探究结果合理的处理了废液。
【反思与总结】
a.通过甲同学实验可知,判断无明显现象的中和反应发生了,可以通过实验验证 _______ 即可;
b.通过上述探究过程可知,猜想反应后溶液中溶质成分时,不仅要考虑可溶于水的反应物及生成物,还要考虑_________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示是A、B两种物质的溶解度曲线,A与B的溶解度曲线相交于P点。据图回答:
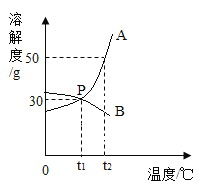
(1)P点处,A、B两物质的溶解度均为____________。
(2)t2°C时,40g的A放置在50g的水中可以配制成___g的溶液。
(3)将P点处A、B溶液升温至t2°C时,所得溶液溶质质量分数的大小关系是___________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知A、B分别是盐酸溶液和氢氧化钠溶液中的一种,如图表示向A中加入B时,溶液的pH变化曲线。

(1)A是________________________;
(2)B是________________________;
(3)C点时溶液中的溶质为__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com