
KCl和KOH的混合物9.26g,将它溶于40.14g水中,然后加入14.6g溶质质量分数为10%的盐酸恰好中和.求:
(1)原混合物中含KOH多少克?
(2)反应后所得氯化钾溶液中,氯化钾的质量分数是多少?
科目:初中化学 来源: 题型:
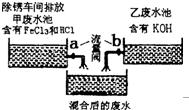 24、课外小组的同学在参观废水处里厂时,得知除锈车间排放到甲废水池中含有的FeCl3、HCl与乙废水池中含有的KOH废水进行混合(如图),课外小组的同学对混合后的废水池中的溶液进行探究.
24、课外小组的同学在参观废水处里厂时,得知除锈车间排放到甲废水池中含有的FeCl3、HCl与乙废水池中含有的KOH废水进行混合(如图),课外小组的同学对混合后的废水池中的溶液进行探究.查看答案和解析>>
科目:初中化学 来源: 题型:
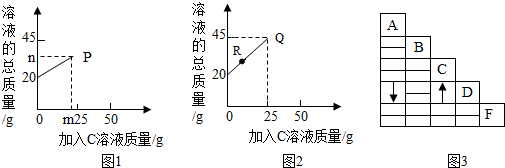
查看答案和解析>>
科目:初中化学 来源: 题型:
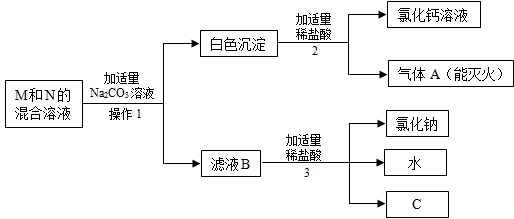
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
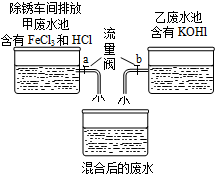 课外小组的同学在参观废水处里厂时,得知除锈车间排放到甲废水池中含有的FeCl3、HCl与乙废水池中含有的KOH废水进行混合(如图),课外小组的同学对混合后的废水池中的溶液进行探究.
课外小组的同学在参观废水处里厂时,得知除锈车间排放到甲废水池中含有的FeCl3、HCl与乙废水池中含有的KOH废水进行混合(如图),课外小组的同学对混合后的废水池中的溶液进行探究.查看答案和解析>>
科目:初中化学 来源:2011年黑龙江省哈尔滨市道外区中考化学一模试卷(解析版) 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com