
科目:初中化学 来源: 题型:解答题
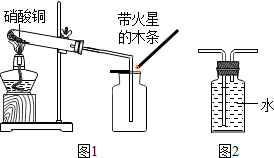 硝酸铜为蓝色固体,溶于水可得蓝色溶液.某实验小组同学用如图装置加热硝酸铜,发现固体由蓝色逐渐变黑,同时产生红棕色有刺激性气味的气体,带火星的木条复燃.
硝酸铜为蓝色固体,溶于水可得蓝色溶液.某实验小组同学用如图装置加热硝酸铜,发现固体由蓝色逐渐变黑,同时产生红棕色有刺激性气味的气体,带火星的木条复燃.| 实验操作 | 实验现象 | 实验结论 |
| 步骤Ⅰ:将反应后试管中的固体加水充分溶解、过滤、将干燥后滤渣加入 稀硫酸溶液中. | 固体全部溶解,得到蓝色溶液 | 硝酸铜分解生成了氧化铜. |
步骤Ⅱ:在图1的试管和集气瓶之间连图所示的装置,重新进行加热硝酸铜的实验.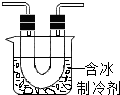 | 集气瓶中气体为无色,带火星木条复燃 | 硝酸铜分解生成了氧气 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 现象:将氢氧化钠溶液加入氯化铜溶液会产生红褐色沉淀 | |
| B. | 设计:验证久置空气的NaOH是否变质,可将固体溶于水并加入酚酞试液观察颜色 | |
| C. | 操作:石蕊试纸和pH试纸使用前都必须用蒸馏水润湿 | |
| D. | 步骤:探究H2还原氧化铜反应时,实验结束时应先移去酒精灯,再停止通H2 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
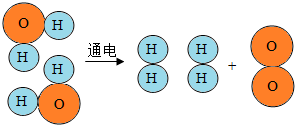 如图是水分子在通电条件下分解的示意图.从图中你可以获得哪些信息,请任写三条:
如图是水分子在通电条件下分解的示意图.从图中你可以获得哪些信息,请任写三条:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com