
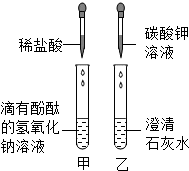
 某校研究学习小组的同学在探究复分解反应发生的条件时,进行了如图所示的实验.
某校研究学习小组的同学在探究复分解反应发生的条件时,进行了如图所示的实验.| 实验内容 | 预计现象 | 预计结论 |
| 取少量废液缸中上层清液于试管中,加入过量的氯化钙溶液,静置. | ①有白色沉淀产生,溶液由红色变无色. | |
| ② |
| 实验内容 | 预计现象 | 预计结论 |
| 取少量废液缸中上层清液于试管中,加入过量的氯化钙溶液,静置. | ①有白色沉淀产生,溶液由红色变无色. 只有碳酸钾 | 小岑的猜想正确 |
| ②没有白色沉淀,溶液呈红色 | 小茜的猜想正确 |


 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案科目:初中化学 来源: 题型:
| A、28.6g | B、23.7g |
| C、20g | D、18.2g |
查看答案和解析>>
科目:初中化学 来源: 题型:
 如图是 A、B、C 三种固体物质的溶解度曲线图,请结合图示回答下列问题:
如图是 A、B、C 三种固体物质的溶解度曲线图,请结合图示回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:
| 实验 序号 |
过氧化氢溶液 浓度/% |
过氧化氢溶液质量/g | 温度/℃ | 二氧化锰用量/g | 氧气体积/ml | 反应所需时间/s |
| ① | 5 | 12 | 20 | 0.2 | 125 | 11 |
| ② | 30 | 12 | 20 | 0.2 | 125 | 2 |
| ③ | 30 | 12 | 4 | / | 125 | 148 |
| ④ | 30 | 12 | 90 | / | 125 | 82 |
查看答案和解析>>
科目:初中化学 来源: 题型:
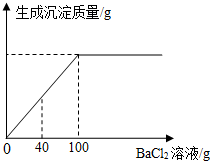 小张同学为了测定某混合物(含Na2CO3和NaOH)中碳酸钠的质量分数.进行了如下实验:现称取了该样品20g配成溶液,然后向该溶液中逐滴加入溶质质量分数为20.8%的BaCl2溶液,生成沉淀的质量与加入BaCl2溶液的质量关系如图所示.
小张同学为了测定某混合物(含Na2CO3和NaOH)中碳酸钠的质量分数.进行了如下实验:现称取了该样品20g配成溶液,然后向该溶液中逐滴加入溶质质量分数为20.8%的BaCl2溶液,生成沉淀的质量与加入BaCl2溶液的质量关系如图所示.查看答案和解析>>
科目:初中化学 来源: 题型:
 实验室所用硫酸试剂瓶上标签的部分内容,请仔细阅读后计算:
实验室所用硫酸试剂瓶上标签的部分内容,请仔细阅读后计算:查看答案和解析>>
科目:初中化学 来源: 题型:
 实验室中有一瓶标签受损的无色液体,如图所示.这瓶无色液体是什么呢?实验员老师告诉大家,该液体只能是过氧化氢溶液、稀硫酸.为确定该液体成分,同学们继续进行了如表实验探究:
实验室中有一瓶标签受损的无色液体,如图所示.这瓶无色液体是什么呢?实验员老师告诉大家,该液体只能是过氧化氢溶液、稀硫酸.为确定该液体成分,同学们继续进行了如表实验探究:| 实验操作 | 实验现象 | 实验结论 |
| 步骤一:取该液体适量于试管中,向其中加入少量 | 没有气泡产生. | 该液体不是过氧化氢溶液. |
| 步骤二:取该液体适量于试管中,向其中滴加少量氯化钡溶液. | 该液体是稀硫酸. |
查看答案和解析>>
科目:初中化学 来源: 题型:
 中和反应是放热反应.取10mL溶质质量分数为10%的NaOH溶液(密度1.10g/mL)置于烧杯中(并滴入2滴酚酞),向烧杯中逐滴加入稀盐酸.随着盐酸的滴入,烧杯中溶液颜色从红色逐渐变浅,当加入10mL稀盐酸时,溶液恰好变为无色.烧杯中溶液温度与加入盐酸体积之间关系如图所示.
中和反应是放热反应.取10mL溶质质量分数为10%的NaOH溶液(密度1.10g/mL)置于烧杯中(并滴入2滴酚酞),向烧杯中逐滴加入稀盐酸.随着盐酸的滴入,烧杯中溶液颜色从红色逐渐变浅,当加入10mL稀盐酸时,溶液恰好变为无色.烧杯中溶液温度与加入盐酸体积之间关系如图所示.查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com