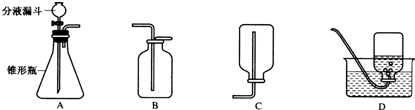
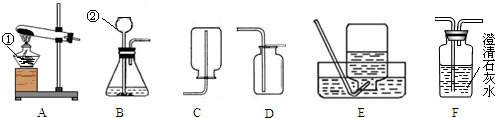
解:(1)由常用仪器的名称可知C装置除了导气管外,还有集气瓶和水槽;
(2)在加入过氧化氢溶液和MnO
2前,应检查装置的气密性;用过氧化氢溶液和MnO
2制取氧气时,由于分液漏斗是用来装液体药品,所以分液漏斗中应放入的物质是过氧化氢(H
2O
2),MnO
2在反应中起催化作用;要收集一瓶纯净的氧气,应选择D 装置;氧气中如含有水蒸气可用浓硫酸来吸收;
(3)用过氧化氢制取氧气的方程式是:2H
2O
2
2H
2O+O
2↑;
(4)某同学在观察到锥形瓶内有大量气泡时,开始用B装置收集氧气,一段时间后,用带火星的木条伸到瓶口,未见木条复燃.其原因可能是装置的气密性不好;
(5)A装置中反应很剧烈,可通过控制双氧水溶液的滴加速度来控制反应的进行.
故答为:(1)集气瓶,水槽;(2)气密,过氧化氢(H
2O
2),催化,D,浓硫酸;(3)2H
2O
2
2H
2O+O
2↑;(4)装置的气密性不好;(5)控制双氧水溶液的滴加速度.
分析:(1)C装置均为实验室常用的仪器,熟记常用仪器的名称即可轻松作答;
(2)制取气体的装置都要检查装置的气密性,根据装置的用途和反应物的状态,确定里面装入的药品,根据二氧化锰的作用分析,要收集一瓶纯净的氧气,应用排水法收集,氧气中如含有水蒸气可用浓硫酸来干燥;
(3)根据用过氧化氢制取氧气的反应写出反应的方程式;
(4)根据实验的过程应注意的事项进行分析原因;
(5)根据影响反应速率的因素进行分析.
点评:本题主要考查气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写和操作中的注意事项,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.


 2H2O+O2↑;
2H2O+O2↑; 2H2O+O2↑;(4)装置的气密性不好;(5)控制双氧水溶液的滴加速度.
2H2O+O2↑;(4)装置的气密性不好;(5)控制双氧水溶液的滴加速度.