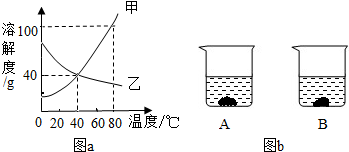
解答:解:(1)由饱和溶液溶质质量分数=
×100%可知,溶解度大,饱和溶液的溶质质量分数就大,t
2℃时,甲物质与乙物质溶解度相等,所以饱和溶液的质量分数也相等;
(2)由溶解度曲线可知甲、乙两种物质的溶解度受温度影响较小的是乙物质;
(3)t
3℃时,乙物质的溶解度是80g,所以在该温度下,100g水中最多溶解80g乙物质,t
3℃时,把100g乙物质放入100g水中,充分搅拌,所得溶液是饱和溶液,且有20g乙没溶解,所得溶液质量为80g+100g=180g;溶质质量分数:
×100%=44.4%;
(4)接近饱和的溶液,变成饱和可以用加入溶质和蒸发溶剂,因为甲的溶解度随温度的升高而增大,所以也可以通过降低温度实现;
(5)从t
1℃向上做垂线,与曲线的交点在上面的溶解度就大,所以t
1℃时甲的溶解度小于乙物质的溶解度;由于饱和溶液溶质质量分数=
×100%可知,溶解度大,饱和溶液的溶质质量分数就大,在t
1℃甲的溶解度小于乙物质的溶解度,所以t
1℃甲物质的饱和溶液的溶质质量分数小于乙物质饱和溶液的质量分数,升温后,甲和乙物质都由饱和溶液变为不饱和溶液,溶质质量分数不变,所以升温后还是甲物质的饱和溶液的溶质质量分数小于乙物质饱和溶液的质量分数;若把t
3℃时甲、乙的饱和溶液分别降温至t
2℃,溶解度都变小,析出晶体,都还是饱和溶液,在t
2℃甲物质和乙物质的溶解度相等,所以饱和溶液的溶质质量分数也相等;
(6)如果溶解度受温度影响较大的物质从溶液中结晶析出的方法是冷却热饱和溶液,如果溶解度受温度影响不大的物质从溶液中结晶析出的方法是蒸发溶剂.由于甲物质的溶解度受温度影响较大,所以提纯甲用降温结晶或冷却热饱和溶液.
故答案为:(1)=;(2)乙;(3)饱和;180g;44.4%;(4)加入溶质(或蒸发溶剂、降低温度);(5)<;<;=;(6)A.

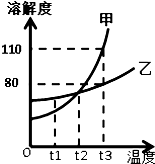 如图所示是甲、乙两固体物质的溶解度曲线,请回答下列问题
如图所示是甲、乙两固体物质的溶解度曲线,请回答下列问题