
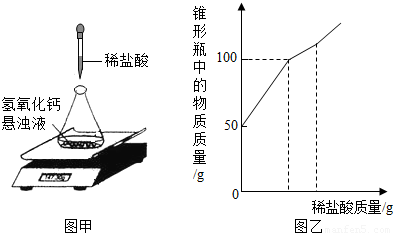
 某研究性学习小组在协助老师清理实验储备室时,发现一批存放多年的氢氧化钙.为检验其变质情况,进行了如下探究:取氢氧化钙样品11.4g于锥形瓶中,加入38.6g水,振荡形成悬浊液,放在电子天平上,向锥形瓶中逐滴滴加14.6%的稀盐酸,振荡后读取质量(如图甲所示).实验测得加入稀盐酸的质量与锥形瓶中物质的质量关系如图乙所示.求:11.4g该样品中各成分的质量.
某研究性学习小组在协助老师清理实验储备室时,发现一批存放多年的氢氧化钙.为检验其变质情况,进行了如下探究:取氢氧化钙样品11.4g于锥形瓶中,加入38.6g水,振荡形成悬浊液,放在电子天平上,向锥形瓶中逐滴滴加14.6%的稀盐酸,振荡后读取质量(如图甲所示).实验测得加入稀盐酸的质量与锥形瓶中物质的质量关系如图乙所示.求:11.4g该样品中各成分的质量.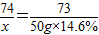


科目:初中化学 来源: 题型:阅读理解

| 实验操作 | 实验现象和结论 |
| 取少量乙溶液于试管中, 在溶液中插入一根铜丝 在溶液中插入一根铜丝 ,观察.或者(取少量乙溶液于试管中, 滴加几滴稀盐酸(或其他氯化物溶液) 滴加几滴稀盐酸(或其他氯化物溶液) ) | 若 铜丝表面无变化 铜丝表面无变化 ,则是Zn(NO3)2、Fe(NO3)2 Zn(NO3)2、Fe(NO3)2 ,若铜丝表面有银白色固体析出 铜丝表面有银白色固体析出 则是Zn(NO3)2、Fe(NO3)2、AgNO3 Zn(NO3)2、Fe(NO3)2、AgNO3 .或者(若 溶液无明显变化 溶液无明显变化 ,则溶质是Zn(NO3)2、Fe(NO3)2 Zn(NO3)2、Fe(NO3)2 ,若溶液中有沉淀生成 溶液中有沉淀生成 ,则溶质是Zn(NO3)2、Fe(NO3)2、AgNO3 Zn(NO3)2、Fe(NO3)2、AgNO3 .) |
查看答案和解析>>
科目:初中化学 来源: 题型:
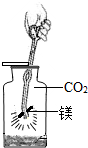 某研究性学习小组在一本参考书上发现,镁居然能在二氧化碳气体中燃烧!于是他们进行了这个实验:将镁条点燃后迅速伸人盛有二氧化碳的集气瓶中,发现镁条剧烈燃烧.发出白光,放热,产生一种白色粉末和一
某研究性学习小组在一本参考书上发现,镁居然能在二氧化碳气体中燃烧!于是他们进行了这个实验:将镁条点燃后迅速伸人盛有二氧化碳的集气瓶中,发现镁条剧烈燃烧.发出白光,放热,产生一种白色粉末和一查看答案和解析>>
科目:初中化学 来源: 题型:
 19、某研究性学习小组在实验中发现:不仅碱溶液可以使酚酞试液变红,Na2CO3溶液也能使酚酞试液变红.碱溶液可以使酚酞试液变红,是因为碱在水中解离出了OH-,那么Na2CO3溶液中究竟是哪种粒子可以使酚酞试液变红呢?他们设计了如图三个实验,请你和他们一起探究并完成下列问题:
19、某研究性学习小组在实验中发现:不仅碱溶液可以使酚酞试液变红,Na2CO3溶液也能使酚酞试液变红.碱溶液可以使酚酞试液变红,是因为碱在水中解离出了OH-,那么Na2CO3溶液中究竟是哪种粒子可以使酚酞试液变红呢?他们设计了如图三个实验,请你和他们一起探究并完成下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| 步骤 | 实验操作 | 实验现象 | 结论 |
| 1 | 取少量样品于试管中,加水完全 溶解,再加入 过量的氯化钙溶液 过量的氯化钙溶液 |
产生白色沉淀 产生白色沉淀 |
丙的猜想 不成立 |
| 2 | 取步骤1反应后的溶液于试管中 滴加酚酞试液 滴加酚酞试液 |
酚酞试液不变色 酚酞试液不变色 |
只有甲的 猜想成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com