
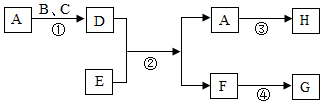
 A-H是初中化学常见物质,其中D、H为红色固体,E为有毒气体,它们之间的转化关系如图所示,回答下列问题:
A-H是初中化学常见物质,其中D、H为红色固体,E为有毒气体,它们之间的转化关系如图所示,回答下列问题:分析 根据D为红色固体,E为一种有毒气体,二者能反应产生A和F,F得到G常用于检验气体F,因此F是二氧化碳,G是碳酸钙;则A是铁,D是氧化铁,E是一氧化碳,B、C是氧气和水;铁经过反应产生的H也是红色固体,因此可能是铁和铜盐反应产生的铜,据此分析.
解答 解:D为红色固体,E为一种有毒气体,二者能反应产生A和F,F得到G常用于检验气体F,因此F是二氧化碳,G是碳酸钙;则A是铁,D是氧化铁,E是一氧化碳,B、C是氧气和水;铁经过反应产生的H也是红色固体,因此可能是铁和铜盐反应产生的铜,如铁和硫酸铜反应产生硫酸亚铁和铜,带入验证符合转化关系,因此:
(1)反应①是铁和氧气、水生锈的过程,可以涂油漆等进行防锈;故填:涂油漆等;
(2)反应②是一氧化碳与氧化铁反应生成铁和二氧化碳,故反应的化学方程式为:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(3)反应④可以是铁和硫酸铜反应生成硫酸亚铁和铜,是单质和化合物反应产生新的单质和新的化合物,属于置换反应;故填:置换反应;
(4)反应④常用于检验气体F,因此是二氧化碳和氢氧化钙的反应,反应的方程式为:CO2+Ca(OH)2═CaCO3↓+H2O,其中钙元素的化合价为+2;故填:+2.
点评 本题为框图式推断题,解题关键是从信息中找准突破口,直接得出答案,然后再顺推或逆推或向中间推的方法推测出其它答案,做出正确解答即可.


 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 该粉末中一定不含有KNO3、CuSO4 | |
| B. | 该粉末的组成中可能含有CuSO4 | |
| C. | 该粉末中一定含有Na2SO4、KNO3、BaCl2 | |
| D. | 粉末中一定含有CaCO3、Na2SO4、BaCl2 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 4:11 | B. | 4:7 | C. | 9:1 | D. | 1:9 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验方案 | 测溶液pH | 滴加Na2CO3溶液 | 滴加AgNO3溶液 |
| 实验操作 |  |  |  |
| 实验现象 | 试纸变色,对比标准比色卡,pH<7 | 产生白色沉淀 | |
| 实验结论 | 溶液中有HCl | 溶液中有HCl | 溶液中有HCl |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com