
分析 (1)根据在化学反应中,反应前后原子的种类和数目不变进行解答;
(2)根据决定元素种类的是质子数;决定元素化学性质的是最外层电子数进行解答;
(3)根据碳元素组成的单质,它们的物理性质存在较大差异的原因是碳原子的排列方式不同;由一种元素组成的物质,可能是单质,也可能是混合物进行解答;
(4)根据木炭与氧化铜反应生成铜和二氧化碳进行解答.
解答 解:(1)在化学反应中,反应前后原子的种类和数目不变;故填:种类和数目;
(2)决定元素种类的是质子数;决定元素化学性质的是最外层电子数,最外层电子数相同元素的化学性质相似;故填:质子数;最外层电子数;
(3)碳元素组成的单质,它们的物理性质存在较大差异的原因是碳原子的排列方式不同;由一种元素组成的物质,可能是单质,也可能是混合物;故填:碳原子的排列方式不同;单质;混合物;
(4)木炭与氧化铜反应生成铜和二氧化碳,反应的化学方程式为:C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑,木炭是反应的还原剂,氧化铜失去氧,发生了还原反应.故填:C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑;C;还原.
点评 本题难度不大,掌握碳具有还原性、木炭还原氧化铜的实验现象与结论等是正确解答本题的关键.


科目:初中化学 来源: 题型:实验探究题
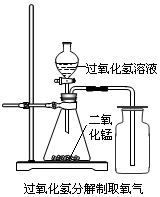 实验室中,常采用分解过氧化氢溶液(二氧化锰作催化剂)或加热高锰酸钾的方法制取氧气.
实验室中,常采用分解过氧化氢溶液(二氧化锰作催化剂)或加热高锰酸钾的方法制取氧气.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验步骤 | 实验现象 | 实验结论 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 混合气体中丙烯(C3H6)的质量分数一定为50% | |
| B. | 消耗O2的质量一定为48 g | |
| C. | 混合气体中碳与氢的质量之比一定是6:1 | |
| D. | 混合气体燃烧生成H2O的质量一定为18 g |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
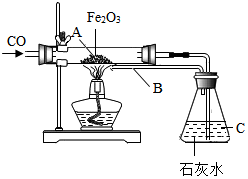 有位同学设计了下列实验(装置及所用药品如图所示),仔细观察后回答下列问题.
有位同学设计了下列实验(装置及所用药品如图所示),仔细观察后回答下列问题.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验.
某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验.| 实验操作 | 实验现象 | 结论 |
| 取少量黄色固体于试管中,加入适量的水,并将湿润的红色石蕊试纸放在试管口. | 试管中有气体产生,湿润的红色石蕊试纸变蓝 | 猜想正确 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com