
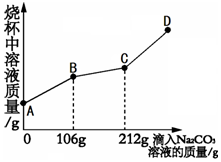
 ��һ�ձ���ʢ��l00��BaCl2��HCl�Ļ����Һ���������μ�������������Ϊ10%��Na2CO3��Һ�������Һ��������������Na2CO3��Һ��������ϵ������ͼ��ʾ������������ʴ����⣺
��һ�ձ���ʢ��l00��BaCl2��HCl�Ļ����Һ���������μ�������������Ϊ10%��Na2CO3��Һ�������Һ��������������Na2CO3��Һ��������ϵ������ͼ��ʾ������������ʴ����⣺���� ��1����ʢ��BaCl2��HCl�Ļ����Һ�еμ�Na2CO3��Һʱ��̼�����������ᷴӦ����������̼�������ᷴӦ��������Ȼ�����Ӧ����̼�ᱵ�������ݴ˷����жϣ�
��2������BC��BaCl2��Һ�е�BaCl2�����Na2CO3��Һ��Ӧ������̼�ᱵ������CD��Һ��BaCl2��HCl����ȫ��Ӧ������Na2CO3��Һ������������Һ���ӵ����������ش�
��3�����ݵ�����Na2CO3��Һ��ͼ��C��ʱ����Һ�е�BaCl2��HCl����ȫ��Ӧ�����ݷ����ķ�Ӧ�����Һ�е��Ȼ��ơ����ɵ�̼�ᱵ���Ͷ�����̼���������ٸ��������غ㶨�ɺ����ʵ����������ļ��㹫ʽ���㣮
��� �⣺��1����һ�ձ���ʢ��l00��BaCl2��HCl�Ļ����Һ���������μ�������������Ϊ10%��Na2CO3��Һ̼��������ϡ���ᷴӦ�����˶�����̼���壬�����ܹ۲쵽������ų�ʵ����������߶���AB�Σ��ʢ���ȷ��
��2����ͼʾ��֪��BC��BaCl2��Һ�е�BaCl2�����Na2CO3��Һ��Ӧ������̼�ᱵ������CD��Һ��BaCl2��HCl����ȫ��Ӧ������Na2CO3��Һ������������Һ���ӵ������������߶�CD�ε�б�ʱ�BC�δ�
��3����ϡ������̼���Ʒ�Ӧ���ɵ��Ȼ��Ƶ�����Ϊx�����ɵĶ�����̼������Ϊy��
Na2CO3+2HCl=2NaCl+CO2��+H2O
106 117 44
106g��10% x y
$\frac{106}{106g��10%}=\frac{117}{x}=\frac{44}{y}$ ��ã�x=11.7g y=4.4g
��3����ͼ���֪��BaCl2��Һ��Ӧ��̼������Һ������Ϊ��216g-106g=106g
��BaCl2��Һ��̼������Һ��Ӧ���ɵ�̼�ᱵ������Ϊm�����ɵ��Ȼ��Ƶ�ֻ���Ǹ�Ϊn
BaCl2+Na2CO3�TBaCO3��+2NaCl
106 197 117
106g��10% m n
$\frac{106}{106g��10%\\;}=\frac{197}{m}=\frac{117}{n}$ ��ã�m=19.7g n=11.7g
����NaCl��Һ����������Ϊ��$\frac{11.7g+11.7g}{100g+212g-19.7g-4.4g}$��100%=8.13%
�ʴ�Ϊ����1���٣���2��BC��BaCl2��Һ�е�BaCl2�����Na2CO3��Һ��Ӧ������̼�ᱵ������CD��Һ��BaCl2��HCl����ȫ��Ӧ������Na2CO3��Һ������������Һ���ӵ���������3����4��������Һ����������������8.13%
���� ���⿼�����ͼ����йػ�ѧ����ʽ�ļ��㣬���ڿ���ѧ����ʶͼ��̼�������������ʶ��ܷ�����Ӧ���������������ᷴӦ��������Ȼ�����Ӧ��������ѣ�ѧ�����׳�����ƽʱҪ��ע��ѵ����


 ��ѧ�̸̳����¿α�ϵ�д�
��ѧ�̸̳����¿α�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ���� | ���� | �����ʵķ��� | |
| A | NaOH��Һ | Ca��OH��2 | ����Na2CO3��Һ������ |
| B | CaCl2��Һ | HCl | ����CaCO3������ |
| C | Zn | Fe | Zn��NO3��2������ |
| D | CO2 | CO | ��ȼ |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
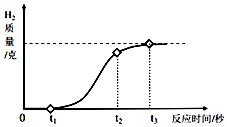 �������ִ������г����İ�װ���ϣ����þ��ˣ�������ɫ�����䰵�������ֳƼ�������
�������ִ������г����İ�װ���ϣ����þ��ˣ�������ɫ�����䰵�������ֳƼ��������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2.2g | B�� | 2.6g | C�� | 3g | D�� | 3.4g |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
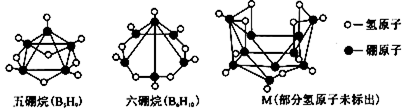
| A�� | ��������6����ԭ�Ӻ�10����ԭ�ӹ��� | |
| B�� | ͼ��M������Ϊ������ | |
| C�� | �����п�����δ���������Դ | |
| D�� | 2B5H9+12O2$\frac{\underline{\;��ȼ\;}}{\;}$5X+9H2O����X��B�Ļ��ϼ�Ϊ+5�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
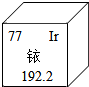 2014��5��7�����Ͼ���ʧ�ķ���Դҿ-192����5��10�հ�ȫ���գ�ҿ-192�Ǹ�Σ����Դ����Σ�����彡������ͼ��ʾ��Ԫ�����ڱ��е�һ���й�˵��������ǣ�������
2014��5��7�����Ͼ���ʧ�ķ���Դҿ-192����5��10�հ�ȫ���գ�ҿ-192�Ǹ�Σ����Դ����Σ�����彡������ͼ��ʾ��Ԫ�����ڱ��е�һ���й�˵��������ǣ�������| A�� | ҿԪ���ǽ���Ԫ�� | |
| B�� | ҿ-192ԭ�ӵ�������Ϊ77��������Ϊ115 | |
| C�� | ҿԪ�ص����ԭ������Ϊ192.2g | |
| D�� | ҿ-192��ҿ-191��ҿ-193����ͬλ��ԭ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� |  | B�� | 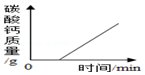 | C�� |  | D�� | 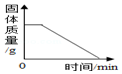 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ${\;}_{8}^{18}$O ��${\;}_{8}^{16}$O ��Ϊͬλ��ԭ�� | |
| B�� | ${\;}_{8}^{18}$O ������������${\;}_{8}^{16}$O | |
| C�� | ${\;}_{8}^{18}$O ��${\;}_{8}^{16}$O ����ͬ��ԭ�� | |
| D�� | ${\;}_{8}^{18}$O ��${\;}_{8}^{16}$O ������������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com