
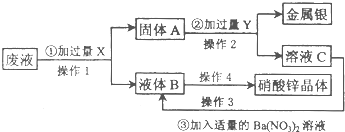
 某工厂排出的废液中主要含有硝酸锌和硝酸银.为了防止环境污染并从中回收金属银和硝酸锌,设计以下方案.回答以下问题;
某工厂排出的废液中主要含有硝酸锌和硝酸银.为了防止环境污染并从中回收金属银和硝酸锌,设计以下方案.回答以下问题;

科目:初中化学 来源: 题型:
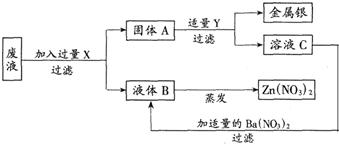
查看答案和解析>>
科目:初中化学 来源: 题型:
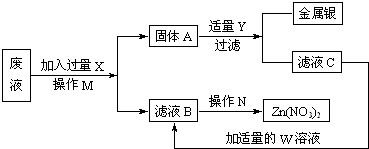
查看答案和解析>>
科目:初中化学 来源:不详 题型:问答题

查看答案和解析>>
科目:初中化学 来源:2006年第十六届“天原杯”全国初中学生化学素质和实验能力竞赛(江苏赛区)初赛试卷(解析版) 题型:解答题
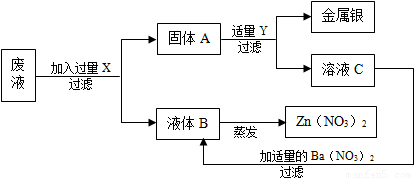
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com