

分析 【探究活动一】
二氧化碳能使澄清石灰变浑浊;
一氧化碳燃烧生成二氧化碳;
高温条件下,铜能和空气中的氧气反应生成氧化铜;
为了防止一氧化碳和空气混合点燃时发生爆炸,加热前应该通入一会儿一氧化碳;
【探究活动二】
红色固体可能是Cu2O和Cu,也可能是Cu2O;
过滤可以把不溶于水的物质除去;
根据提供的数据可以计算氧化亚铜的质量;
如果操作不当,会影响实验结果,甚至会导致实验失败;
加热条件下,氧化铜和一氧化碳反应生成铜和二氧化碳.
解答 解:【探究活动一】
①实验过程中,C中的现象是澄清石灰水变浑浊,D处点燃的目的是把一氧化碳转化成二氧化碳,D处发生的反应方程式为:2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2.
故填:澄清石灰水变浑浊;把一氧化碳转化成二氧化碳;2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2.
②A.实验结束时应先熄灭B处酒精灯,继续通入一氧化碳直至冷却至室温,该选项说法正确;
B.C中增加的质量与B中固体减小的质量不相等,C中增加的质量大于B中固体减小的质量,该选项说法不正确;
C.因为一氧化碳不能完全反应,因此实验中若通入28g一氧化碳时,生成铜的质量小于64g,该选项说法不正确;
D.反应结束后继续通入一氧化碳的目的之一是防止铜被氧化,该选项说法正确.
故填:AD.
③甲同学认为A装置用于证明一氧化碳不能和石灰水反应,乙同学认为省略A可达到同样的目的,理由是为了排尽装置中的空气,反应前已经通入一定量的一氧化碳,过程中C中的澄清石灰水不变浑浊,说明一氧化碳不能和石灰水反应.
故填:为了排尽装置中的空气,反应前已经通入一定量的一氧化碳.
【探究活动二】
猜想①:是Cu2O和Cu;猜想②:是Cu2O.
故填:Cu2O.
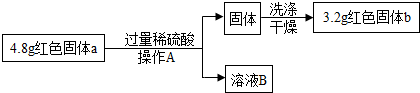
①操作A为过滤,加过量硫酸的目的是使氧化亚铜完全反应,溶液B中含有的溶质是过量的硫酸和生成的硫酸铜,洗涤的目的是除去铜表面的杂质.
故填:过滤;使氧化亚铜完全反应;硫酸、硫酸铜;除去铜表面的杂质.
②设氧化亚铜质量为x,
Cu2O+H2SO4=CuSO4+Cu+H2O,
144 64
x $\frac{64}{144}$x
根据题意有:4.8g-x+$\frac{64}{144}$x=3.2g,
x=2.88g,
故填:2.88g.
③A.稀硫酸量不足,氧化亚铜不能完全反应,会导致红色固体a中Cu2O的质量分数偏小;
B.反应后未洗涤剩余的红色固体就直接进行了干燥,导致铜的质量偏大,从而导致红色固体a中Cu2O的质量分数偏小;
C.采用加热烘干的方式干燥剩余红色固体时,铜能和氧气反应生成氧化铜,导致铜的质量偏大,从而导致红色固体a中Cu2O的质量分数偏小;
D.将红色固体b转移到天平上时有少量洒落,导致铜的质量偏小,从而导致红色固体a中Cu2O的质量分数偏大.
故填:ABC.
高温条件下,氧化铜和一氧化碳反应生成铜和二氧化碳,反应的化学方程式为:CuO+CO$\frac{\underline{\;高温\;}}{\;}$Cu+CO2.
故填:CuO+CO$\frac{\underline{\;高温\;}}{\;}$Cu+CO2.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | N2:表示氮气由2个氮原子构成 | B. | FeO:表示氧化铁这种物质 | ||
| C. | Fe2+:可以表示一个铁离子 | D. | Ne:可以表示一个氖原子 |
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | 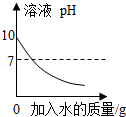 常温下向pH=10的纯碱溶液中不断加入水稀释 | |
| B. |  向等质量的铝粉和镁粉中分别滴入质量相同的足量的稀盐酸 | |
| C. |  等质量的块状石灰石和粉末状石灰石分别与质量分数相同的足量的稀盐酸反应 | |
| D. | 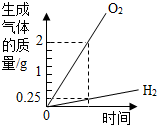 电解水时生成的气体气量比 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 分子可以构成物质,而原子只能构成分子 | |
| B. | 在化学变化中,分子可以分成原子,而原子不能再分 | |
| C. | 原子的质量主要集中在原子核上 | |
| D. | 由分子构成的物质,分子是保持物质化学性质的最小粒子 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Cu和Mg | B. | Ag和Cu | C. | Zn和Cu | D. | Ag |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com