
| 选项 | 事实 | 解释 |
| A | 墙内开花墙外可嗅到花香 | 分子不断运动 |
| B | 空气是混合物 | 由不同种分子构成 |
| C | 水结成冰后体积不变 | 液态水分子之间无间隔,结为冰时分子间有间隔 |
| D | 氮气化学性质不活泼,氧气化学性质较活泼 | 不同分子的化学性质不同 |
分析 根据分子的基本特征:分子质量和体积都很小;分子之间有间隔;分子是在不断运动的;同种的分子性质相同,不同种的分子性质不同,可以简记为:“两小运间,同同不不”,结合事实进行分析判断即可.
解答 解:A、墙内开花墙外可嗅到花香,是因为花香中含有的分子是在不断运动的,向四周扩散,使人们闻到花香,故选项解释正确.
B、空气是混合物,是因为空气中含有氮分子、氧分子、二氧化碳分子等,是由不同种分子构成的,故选项解释正确.
C、液体、气体分子间均有间隔,故选项解释错误.
D、氮气化学性质不活泼,氧气化学性质较活泼,是因为它们分子的构成不同,不同种的分子性质不同,故选项解释正确.
故答案为:C.
点评 本题难度不大,掌握分子的基本性质(可以简记为:“两小运间,同同不不”)及利用分子的基本性质分析和解决问题的方法是解答此类题的关键.


科目:初中化学 来源: 题型:推断题
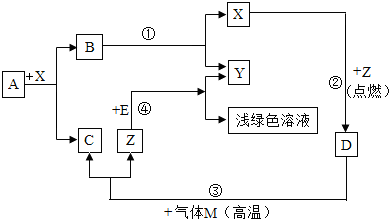
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 小林仔细阅读加碘自然盐包装袋上的说明(部分说明如图所示),提出问题与同学讨论并进行实验探究.
小林仔细阅读加碘自然盐包装袋上的说明(部分说明如图所示),提出问题与同学讨论并进行实验探究.| 温度 | 30℃水浴 | 50℃水浴 | 80℃水浴 | 100℃水浴 | 煮沸 |
| 碘损失率(%) | 0 | 0.3 | 0.67 | 1 | 5.56 |
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | 氢气具有还原性,在反应中被还原 | |
| B. | 氧化铜具有氧化性,在反应中被还原 | |
| C. | 氢气具有可燃性,是理想的燃料 | |
| D. | 氧化反应不一定是物质与氧气的反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | 反应后产生氢气的质量可能相等 | |
| B. | 反应后产生的氢气的质量不相等 | |
| C. | 与金属反应的稀硫酸溶液的质量可能相等 | |
| D. | 与金属反应的稀硫酸溶液质量为:Mg>Fe>Zn |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
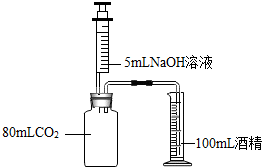 下列三个实验均可证明CO2能与NaOH溶液反应.
下列三个实验均可证明CO2能与NaOH溶液反应.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com