

���� ��1���ٸ���ƿ��ȡ�º�Ҫ���ŵ�ԭ����ʱ���������ԭ������жϣ�
�ڸ���ʵ��IJ������������������ļ��㹫ʽ�����жϣ�
��2�������������������ļ��㹫ʽ������
��3�����ݻ��������������жϣ�
��� �⣺��1����a��ƿ���������������ϣ�b�г������������ŷ��ˣ�
��A����������NaCl����ʱ������ƽָ����������б��������ʵ����ˣ�����������������ƫ��A���������⣻
B��c���ձ���ˮϴ�Ӻ�δ�����ʹ�ã��ܼ�������ƫ�࣬����������������ƫ�ͣ���B�������⣻
C��d�����и�����Ͳ��Һ����ʹ���������ȡ��ˮ���ˣ�����������������ƫ��C���������⣻
D��ת������õ���Һʱ����������Һ������ƿ�⣬����������������Ӱ�죬��D���������⣮
��2����Ҫʳ�ε�����Ϊ��50g��15%=7.5g����Ҫˮ������Ϊ50g-7.5g=42.5g��������ʱ�����Ȼ��Ʒŵ������̣�1g���������룩��ʵ�ʳ�����ʳ�ε�����Ϊ6.5g��ʵ����������Һ�����ʵ����������ǣ�
$\frac{6.5g}{6.5g+42.5g}��100%$��13.3%
��3���Ȼ���ע����Һ���о�һ�ȶ��ԣ�������Һ
A�����������Һ�����Ȼ���ע����Һ��Ϊͬһ�ࣻ
B����ˮ��������Һ�����Ȼ���ע����Һ�鲻Ϊͬһ�ࣻ
C����ˮΪ��������Ȼ���ע����Һ�鲻Ϊͬһ�ࣻ
D��ţ����������Һ�����Ȼ���ע����Һ�鲻Ϊͬһ�࣮
�ʴ�Ϊ��1����a��ƿ���������������ϣ�b�г������������ŷ��ˣ���B����2��6.5��13.3%����3��A��
���� ��ȡҺ��ʱ�����Ӷ�������������λ��Һ���·���ʹ����С��ʵ�����������ʱ������λ��Һ�����϶�ʹ��������ʵ�������


 �̲�ȫ���ִʾ�ƪϵ�д�
�̲�ȫ���ִʾ�ƪϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
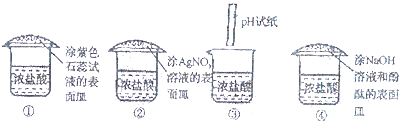
| A�� | �٢ۢ� | B�� | �ڢ� | C�� | �٢ڢ� | D�� | �٢� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
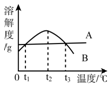
| A�� | t1��ʱ��B��A����Һ�����ʵ������������ | |
| B�� | t2��ʱ��B������Һ�������¶������ǽ��;��о������� | |
| C�� | t2��ʱ��B������Һ���º��Ϊ��������Һ | |
| D�� | t2��ʱ��A������Һ������t3��ʱ�����ʵ������������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 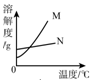 | B�� | 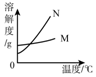 | C�� | 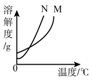 | D�� | 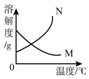 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ͭ��Һ��ͭ���Ӻ���������ӵĵ��������� | |
| B�� | CuSO4•5H2O��һ������Ļ���� | |
| C�� | ������ˮ�ܱ���ɫ���ʿ��õ���������ˮ�Ĵ��� | |
| D�� | �����Ʒ�������ͭ��Һ���к�ɫ��ͭ���û��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ��̽����
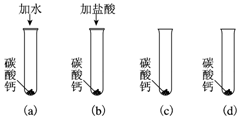
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com