
| A. | 粗盐潮解 | B. | 水果腐烂 | C. | 蔗糖溶解 | D. | 酒精挥发 |
科目:初中化学 来源: 题型:解答题
 金属和金属的化合物在生活、生产中用途广泛.
金属和金属的化合物在生活、生产中用途广泛. ”形状,将锡箔纸的两端连接电池的正负极,锡箔纸即可燃烧.上述实验利用了金属的导电性.
”形状,将锡箔纸的两端连接电池的正负极,锡箔纸即可燃烧.上述实验利用了金属的导电性.查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 地壳中含量最高的金属元素是铁 | B. | 铝的活动性和抗腐蚀性都比铁强 | ||
| C. | 饱和溶液一定比不饱和溶液浓 | D. | 溶液都是均一、稳定的无色液体 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题

| A. | ①和④两种粒子的化学性质相似 | B. | ②和③表示的粒子均为离子 | ||
| C. | ③和④属于同种元素的不同粒子 | D. | ③表示的粒子的符号为Mg+2 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 明矾和二氧化氯均可用作净水剂,所以净水原理相同 | |
| B. | 组成CO和CO2的元素相同,但它们的分子构成不同,所以它们的化学性质不同 | |
| C. | NaOH和CaO溶于水时均能放出热量,是因为它们都能和水发生反应 | |
| D. | 浓盐酸、浓硫酸敞口放置后质量分数都会变小,是因为它们都有挥发性 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 葡萄糖是有机化合物 | |
| B. | 葡萄糖由碳、氢、氧三种元素组成 | |
| C. | 葡萄糖中碳、氢、氧三种元素的质量比为6:1:8 | |
| D. | 葡萄糖的相对分子质量是180g |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
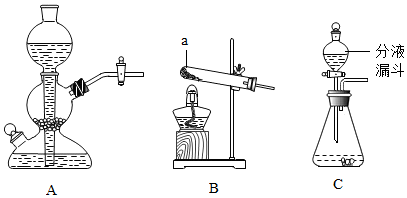
| 甲 | 乙 | 丙 | 丁 | |
| 大理石 | mg,块状 | mg,块状 | mg,粉末状 | mg,粉末状 |
| 盐酸(过量) | wg,稀盐酸 | wg,浓盐酸 | wg,稀盐酸 | wg,浓盐酸 |
| 目的 | 原料 | 发生装置 | 气体较平稳产生的最主要的一个原因 |
| 制取二氧化碳 | 块状大理石稀盐酸 | A | 固体药品的状态和溶液的浓度有关 |
| 制取氧气 | 粉末状二氧化锰3%的过氧化氢溶液 | C | 二氧化锰起催化作用 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com