
分析 (1)根据混合物的定义解答即可;
(2)据氧气的助燃性分析解答;
(3)根据溶液的pH<7,显酸性,pH=7,显中性,pH>7,显碱性解答.
解答 解:(1)洁净的空气属于混合物;
(2)液氧和液氢剧烈燃烧反应所产生的巨大推力使火箭上升.在该化学反应中,液氧所起的作用是支持液氢燃烧,起助燃的作用;
(3)溶液的pH<7,显酸性,pH=7,显中性,pH>7,显碱性,验室用pH试纸测得自来水的pH=8,说明该自来水显碱性;
氧气和臭氧属于不同的物质,所以氧气转化为臭氧属于化学变化;
故答案为:(1)混合物 (2)助燃(或支持燃烧) (3)碱、化学
点评 本题难度不大,考查学生氧气的化学性质,据题意分析解答即可.


科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
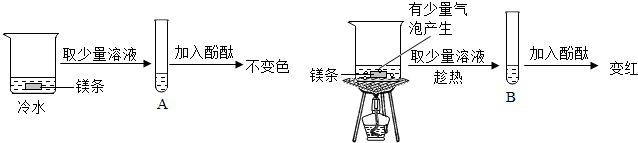
| 猜想 | 验证方案 |
| 可能是氢氧化镁的溶解度受温度的影响,温度降低,溶解度变小,从而导致溶液碱性减弱 | 将褪色后的溶液加热,如果溶液变红,说明小丁的猜想正确 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验步骤 | 实验现象 | 实验结论 |
| (1)取适量电石加水反应,收集生成的气体,验纯后点燃. | 气体燃烧,产生黄色火焰并伴有浓烈黑烟. | 电石与水反应产生的气体是乙炔 |
| (2)取适量反应后生成的固体于试管中,滴加过量稀盐酸. | 固体溶解,没有气体产生. | 电石与水反应产生的固体不是碳酸钙 |
| (3)取适量反应后生成的固体于试管中加水,向上层清液中滴加2~3滴酚酞. | 溶液变红 | 电石与水反应产生的固体是氢氧化钙 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 温度(℃) | 0 | 10 | 20 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
| KNO3 | 13.3 | 20.9 | 32 | 64 | 85.5 | 110 | 138 | 169 | 202 | 246 |
| NaCl | 35.7 | 35.8 | 36 | 36.6 | 37 | 37.3 | 37.8 | 38.4 | 39 | 39.8 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
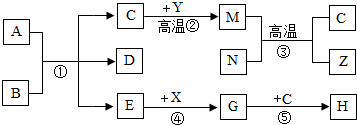
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com