
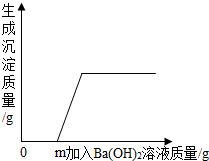
 某溶液由氯化钾溶液、稀硝酸、稀硫酸和硝酸铜溶液中的一种或几种混合而成.取一定量该溶液,向其中滴加Ba(OH)2溶液,生成沉淀的质量与加入Ba(OH)2溶液质量的关系如图所示.
某溶液由氯化钾溶液、稀硝酸、稀硫酸和硝酸铜溶液中的一种或几种混合而成.取一定量该溶液,向其中滴加Ba(OH)2溶液,生成沉淀的质量与加入Ba(OH)2溶液质量的关系如图所示.分析 (1)根据氢氧化钡会与硫酸生成硫酸钡沉淀,氢氧化钡会与酸发生中和反应进行分析;
(2)根据硫酸和氢氧化钡接触就会生成沉淀进行分析.
解答 解:由图象知,加入加入Ba(OH)2溶液不能马上产生沉淀,说明溶液中没有稀硫酸,同时也获悉,溶液显酸性,与生成的沉淀反应,沉淀消失,说明溶液中有稀硝酸;后来加入Ba(OH)2溶液生成沉淀,证明有硝酸铜与氢氧化钡反应生成沉淀,
(1)当加入Ba(OH)2溶液的质量小于m时,沉淀量为零,说明在该段时间没有生成沉淀,故答案为:没有;
(2)硫酸和氢氧化钡接触就会生成沉淀,但是沉淀的量不是加入氢氧化钡就生成了沉淀,所以不存在硫酸,故答案为:H2SO4.
点评 在解此类题时,要学会认知图象,根据图象中的数据进行分析存在的物质和不存在的物质,然后结合推出的物质再验证其他的物质.


科目:初中化学 来源: 题型:解答题
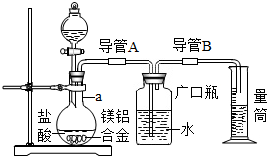 含镁3%~5%的镁铝合金是轮船制造、化工生产、机械制造等行业的重要原材料.现有一块质量为wg的镁铝合金,某研究性学习小组欲测定其中镁的质量分数.
含镁3%~5%的镁铝合金是轮船制造、化工生产、机械制造等行业的重要原材料.现有一块质量为wg的镁铝合金,某研究性学习小组欲测定其中镁的质量分数.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 在一次用餐中,同学们对燃料“固体酒精”产生了好奇,于是对其成分进行研究.
在一次用餐中,同学们对燃料“固体酒精”产生了好奇,于是对其成分进行研究.| 方案 | 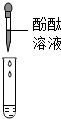 |  |
| 现象 | 溶液变红 | 产生白色沉淀 |
| 结论 | 清液有氢氧化钠 | 清液有碳酸钠 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用带火星的木条伸入集气瓶中检验氧气是否收集满 | |
| B. | 与灯泡串联的开关安装在火线上 | |
| C. | 稀释浓硫酸时,把水沿杯壁倒入浓硫酸中 | |
| D. | 用测电笔辨别火线与零线时,手不接触测电笔的金属体 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
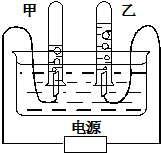 如图表示电解水的简易装置.请回答下列问题:
如图表示电解水的简易装置.请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com