
【题目】有一包不纯的碳酸钾粉末,所含杂质可能是硝酸钾、硝酸钙、氯化钾、氯化亚铁、碳酸钠中的一种或几种。为确定其成分,进行如下实验:
①取少量该粉末于试管中,加足量的水充分溶解,得到无色澄清溶液。向该溶液中加入适量的硝酸银溶液,有白色沉淀产生,再加入足量的稀硝酸,充分反应后,部分白色沉淀消失。
②另取13.8g该粉末于烧杯中,加水使其完全溶解,再加入200g一定溶质质量分数的氯化钡溶液,恰好完全反应,过滤后得到19.7g白色沉淀和滤液a。
下列说法正确的
A. 杂质中一定含有氯化钾,可能含有硝酸钾、碳酸钠
B. 该包粉末的组成只有两种情况
C. 滤液a中所含氯元素质量一定大于7.1g
D. 所用氯化钡溶液中溶质的质量分数为20.8%
【答案】BC
【解析】
①氯化亚铁溶于水溶液呈浅绿色,得到无色澄清溶液,说明粉末中一定不含氯化亚铁和硝酸钙;加入适量的硝酸银溶液,硝酸银能和氯离子反应生成难溶于水且难溶于稀硝酸的白色沉淀氯化银,还能和碳酸根离子反应生成白色沉淀碳酸银,碳酸银难溶于水可溶于酸,根据加入足量的稀硝酸后,部分白色沉淀消失说明粉末中一定含有氯化钾和碳酸钠;由上分析可知样品碳酸钾粉末中一定含有杂质碳酸钠、氯化钾,一定不含氯化亚铁,可能含有硝酸钾;
②根据生成沉淀碳酸钡的质量为19.7g, ![]() ,
,![]() ,再根据方程式中BaCl2~BaCO3的质量比可知,设生成19.7g碳酸钡沉淀消耗氯化钡的质量为x。
,再根据方程式中BaCl2~BaCO3的质量比可知,设生成19.7g碳酸钡沉淀消耗氯化钡的质量为x。
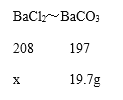
x=20.8g,则所用氯化钡溶液中溶质的质量分数=![]() ×100%=10.4%,氯化钡中含有的氯元素质量=20.8g×
×100%=10.4%,氯化钡中含有的氯元素质量=20.8g×![]() ×100%=7.1g,又因为粉末中一定含有氯化钾,所以滤液a中所含氯元素质量一定大于7.1g。
×100%=7.1g,又因为粉末中一定含有氯化钾,所以滤液a中所含氯元素质量一定大于7.1g。
A、由上分析可知,杂质中一定含有氯化钾、碳酸钠,可能含有硝酸钾,故选项不正确;
B、由上分析可知,该包粉末的组成只有两种情况,一是碳酸钾和碳酸钠和氯化钾和硝酸钾,二是碳酸钾和碳酸钠和氯化钾,故选项正确;
C、由上分析可知,滤液a中所含氯元素质量一定大于7.1g,故选项正确;
D、由上分析可知,所用氯化钡溶液中溶质的质量分数为10.4%,故选项不正确;
故选BC。


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
【题目】下列通过实验得出的结论,其中不合理的是
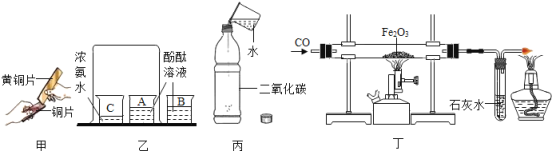
A. 甲实验中黄铜片能在铜片上刻画出痕迹,说明合金的硬度比组成的纯金属大
B. 乙实验不但可以说明分子在不停地运动,还能说明氨水能使无色酚酞变红色
C. 丙实验既可以说明二氧化碳易溶于水,又可以说明二氧化碳能与水反应生成碳酸
D. 丁实验说明一氧化碳具有还原性、可燃性
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学兴趣小组同学用红磷燃烧的方法对空气中氧气的含量进行测定,实验过程中红磷足量、装置气密性良好、操作规范,实验结束后测定结果却低于20%,用测定氧气浓度的传感器测得反应后装置内氧气浓度为8.85%。小组同学查阅资料后改用足量白磷进行实验,测得反应后装置内氧气浓度为3.21%。请回答下列问题:
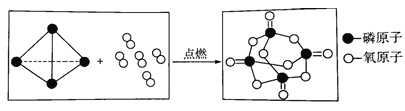
(1)白磷燃烧的微观示意图如图,写出白磷燃烧的化学方程式_____。
(2)采用教材装置测定空气中氧气含量时,改用白磷能使测定结果更准确的原因是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】⑴水是生命的源泉,也是不可缺少的资源。
①自然界的水常遭到污染,污染物中氮和磷含量过高会造成水中藻类过度繁殖,使水质恶化,这里的“氮和磷”是指____;(填字母)
A.元素 B.原子 C.离子 D.分子
②生活中,既能降低水的硬度,又能杀菌消毒的方法是______。
③电解水的装置如下图所示,管A、管B中的气体的质量比是______,在电解水的过程中,保持不变的粒子是____ 。

⑵多彩的“碳”,多姿的生活,让我们一起走进“碳”的世界。
①根据下表提供的信息,填写有关含碳物质的对应特性。
物质用途 | 金刚石切割玻璃 | 活性炭净水 |
对应特性 | __ | __ |
②二氧化碳是一种宝贵的资源。固定和利用二氧化碳的一个成功范例是:CO2+2M===CO(NH2)2+H2O,物质M的化学式为_________。
③目前,人类以化石燃料为主要能源。化石燃料有煤、石油和____,石油主要含有____元素。
⑶铝、铁、铜是人类广泛使用的三种金属,与我们生活息息相关。
①按人类开始使用这三种金属的先后排序为_____(用元素符号表示)。
②在空气中______制品(填“铝”或“铁”)更耐腐蚀。
③用铝和一种化合物的溶液来证明铝和铁的金属活动性强弱,你认为该化合物可以是_______(填化学式)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】利用能源、节约能源、保护环境是我们大家共同关注的社会问题。某工厂将矿物燃料燃烧产生的废气中的SO2收集起来,既可以生产稀硫酸,又能制备氢气。其反应过程如下图所示:
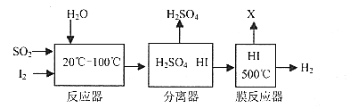
(1)写出反应器中发生化学反应的方程式____________________。
(2)此制备过程中可循环利用的物质是__________。
(3)硫酸用途广泛,汽车铅酸蓄电池中含有硫酸,其中需要用到溶质质量分数为24.5%的硫酸溶液。
①同学们在实验室用浓硫酸配制稀硫酸,除用到胶头滴管、量筒、烧杯外,还需要用到的仪器有___________。
②实验室用98%的浓硫酸(密度1.84g/mL)配制24.5%的硫酸溶液1200g,需要98%浓硫酸的体积为________mL(计算结果保留至0.1)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】以下是初中化学常见实验,请回答有关问题。

(1) 实验一的集气瓶中预先加入了少量水,其作用是__________;
(2) 实验二为电解水的实验,其中A是与电源的_________极相连。通电后,发生反应的符号(或文字)表达 式为:_________________;实验刚开始时,X和Y气体的体积比>2:1,则可能原因是:_____________(填序号);
①氧气溶解的更多 ②氢气溶解的更多 ③氧气密度大 ④氢气密度小 ⑤氧气与电极发生了反应 ⑥水中未加入少量硫酸钠或氢氧化钠
(3) 实验三是测定空气中的氧气含量1/5,假如集气瓶容积为100mL,实验前已经装水20mL,则实验后集气瓶内的水约是_________mL。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在对蜡烛及其燃烧进行了探究以后,请你填写下列空格:
(1)取一支蜡烛,用小刀切下一小块,把它放入水中,蜡烛会___.结论:石蜡的密度比水___;你还能得到蜡烛的物理性质有___.
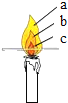
(2)点燃蜡烛,观察到蜡烛火焰分为三层,分别是___、___、___,把一根火柴梗放在蜡烛的火焰上约1s后取出,可以看到___处(填字母)的火柴梗最先碳化.结论:蜡烛火焰的___温度最高.
(3)再将一只干燥的烧杯罩在蜡烛火焰的上方,烧杯内壁出现___,片刻后取下烧杯,迅速向烧杯内倒入少量的澄清石灰水,振荡后发现___.结论;蜡烛燃烧以后的生成物是___.
(4)通过对蜡烛燃烧的观察,你认为蜡烛燃烧发生的变化类型是___.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是几种粒子的结构示意图,有关说法正确的是( )
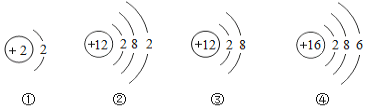
A. 只有①达到了稳定结构
B. ①②元素具有相似的化学性质
C. ②失去电子以后形成的是阳离子
D. ④属于金属元素
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com