
分析 (1)因为生成的氧气逸出,所以根据质量守恒定律“参加反应前各物质的质量总和等于反应后生成各物质的质量总和”可知,生成氧气的质量=反应前溶液质量-反应后剩余物质的总质量;
(2)根据化学方程式得出各物质之间的质量比,即可列出求解过氧化氢质量;
(3)根据(2)中计算出参与反应的过氧化氢质量,然后根据溶质质量分数公式计算即可.
(4)根据溶质一定,列出方程式,即可计算出需加入水的质量
解答 解:(1)根据质量守恒定律,生成氧气的质量为:68g+4g-68.8g=3.2g.
故答案为:质量守恒定律;3.2g.
(2)设参与反应的过氧化氢质量为x,
2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑
68 32
x 3.2g
∴$\frac{68}{x}=\frac{32}{3.2g}$.
故x=6.8g.
答:此瓶中过氧化氢溶液的溶质质量6.8g;
(3)过氧化氢溶液中溶质的质量分数为:$\frac{6.8g}{68g}$×100%=10%.
答:过氧化氢溶液中溶质的质量分数为10%.
(4)设需要瓶内的过氧化氢溶液的质量为y,
则10%y=100g×5%,
解之得:y=50g,
需加入水的质量=100g-50g=50g.则需水的体积为50mL.
答:需要此溶液的质量为50g;加水50毫升.
点评 本题主要考查学生运用化学方程式和质量分数公式进行计算的能力.


 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案科目:初中化学 来源: 题型:解答题
 表示氮原子,
表示氮原子, 表示氢原子,
表示氢原子, 表示催化剂).符合上述反应过程的顺序是D(填字母序号).
表示催化剂).符合上述反应过程的顺序是D(填字母序号).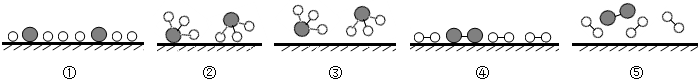
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
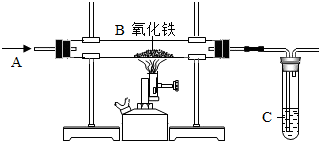 某小组模拟高炉炼铁的化学反应原理进行实验,其装置如图所示,请回答下列问题.
某小组模拟高炉炼铁的化学反应原理进行实验,其装置如图所示,请回答下列问题.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 由两个钠原子和两个氧原子组成 | B. | 由两个钠原子和一个氧分子组成 | ||
| C. | 由两个钠原子和一个氧元素组成 | D. | 由钠、氧两种元素组成 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
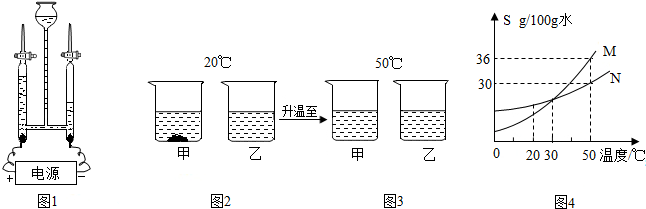
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
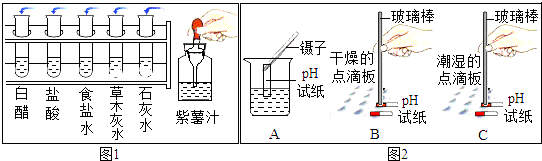
| 溶液 | 白醋 | 盐酸 | 食盐水 | 草木灰水 | 石灰水 |
| 加入紫薯汁后的颜色 | 红色 | 红色 | 紫色 | 绿色 | 绿色 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
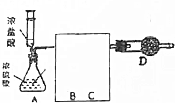 某化学兴趣小组的同学对氯化氢与盐酸的化学性质是否相同进行了探究.
某化学兴趣小组的同学对氯化氢与盐酸的化学性质是否相同进行了探究.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com