
| A.小明用木炭代替红磷做测定空气中氧气含量的实验 |
| B.小颖用锌、铁、铜和稀盐酸确定锌、铁、铜三种金属的活动性 |
| C.小聪在20℃配制36%的氯化钠溶液(20℃时氯化钠的溶解度为36 g) |
| D.小青将过量的木炭粉和少量氧化铜粉的混合物置于蒸发皿里加强热,得到纯净的铜 |
 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源:不详 题型:实验题
| A.烧碱易吸水潮解 | B.烧碱易吸收空气中的CO2而变质 |
| C.烧碱具有强腐蚀性 | D.烧碱溶于水时放出热量 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
| | Zn(OH)2 | Fe(OH)2 | Mg(OH)2 |
| 开始沉淀的pH | 5.7 | 7.6 | 10.4 |
| 沉淀完全的pH | 8.0 | 9.6 | 12.4 |
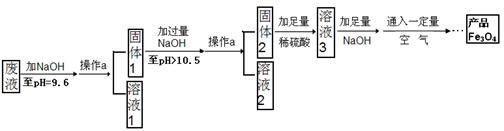
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
| | B | C | D | E |
| A | 无明显变化 | 液体变红色 | 无明显变化 | 白色沉淀 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题

| 实验操作 | 实验现象 | 实验结论 |
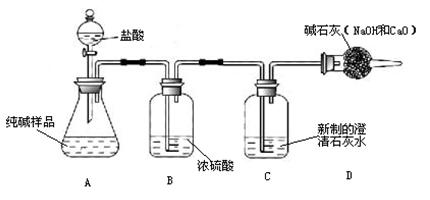
| ⑴取少量固体放于试管中,加足量蒸馏水溶解,静置后取上层清液滴加无色酚酞溶液。 | 固体溶解时试管外壁发烫,试管底部有不溶物,溶液变红。 | 固体中一定含有 ① 和氢氧化钙。 |
| ⑵另取少量固体放于试管中,滴加足量稀盐酸。 | 固体逐渐消失,有大量无色气体产生,得到浅绿色溶液。 | 固体中一定含有 ② , 一定不含Fe2O3。 |
| ⑶将步骤⑵中产生的气体通入到澄清的石灰水中。 | ③ | 固体中一定含有CaCO3。 |

查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
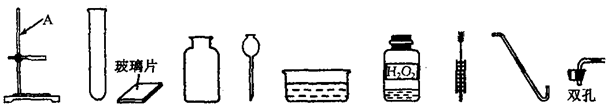
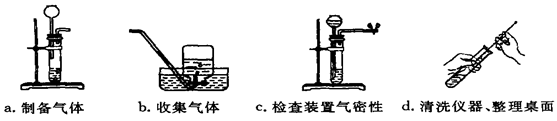
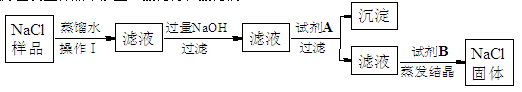
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
| 实验操作 | 实验现象 | 实验结论及分析 |
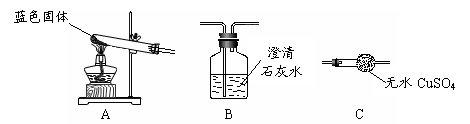
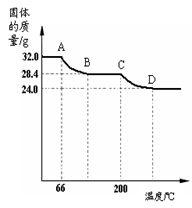
| I.取少量该固体粉末于烧杯中,加入足量的水溶解、过滤 | 粉末部分溶解,得到白色滤渣和无色滤液 | 滤渣中一定含有 |
| Ⅱ.向滤液中粉末部分溶解,得到白色滤渣试液 | 溶液变红 | 滤液中可能含有 物质(填“酸性”、“碱性”或“中性”) |
| Ⅲ.向Ⅱ中所得溶液滴加足量稀盐酸 | | 原固体粉末中一定含有Na2CO3 |

查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com