
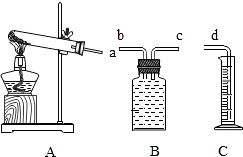
分析 (1)依据碳酸钙和稀盐酸反应生成氯化钙、二氧化碳和水,结合化学方程式的书写方法进行解答;
(2)二氧化碳与水反应生成碳酸,碳酸紫色石蕊试液变红;
(3)在用氯酸钾和二氧化锰制氧气的实验中,二氧化锰的作用是催化作用或加快反应速度;如果测量氧气体积,连接顺序是:a→b→c→d,F装置内应该b管短c管长,根据质量守恒定律可以计算出生成的氧气的质量;
(4)根据收集氧气的注意事项来分析.
解答 解:(1)因为大理石和稀盐酸反应生成氯化钙、水和二氧化碳,故其反应的化学方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑.故填:CaCO3+2HCl═CaCl2+H2O+CO2↑;
(2)二氧化碳与水反应生成碳酸,碳酸能使紫色石蕊试液变红,反应的化学方程式为:CO2+H2O═H2CO3.故填:红;
(3)①二氧化锰的作用是催化作用或加快反应速度;故填:作催化剂;
②如果测量氧气体积,连接顺序是:a→b→c→d,F装置内应该b管短c管长;故填: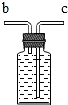 ;
;
③氯酸钾在二氧化锰的催化作用下生成氯化钾和氧气,反应的化学方程式为:2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2KCl+3O2↑.KClO3的相对分子质量为:39+35.5+16×3=122.5;
设生成氧气的质量为x,则
2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2KCl+3O2↑
245 96
12.25g x
$\frac{245}{96}=\frac{12.25g}{x}$
x=4.8g
故答案为:2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2KCl+3O2↑;122.5;4.8;
(4)如果实际测得氧气的体积大于理论值,原因可能是一加热就开始收集氧气.故填:一加热就开始收集氧气.
点评 本考点主要考查气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写和有关的计算等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,要总体把握,本考点主要出现在实验题中.


科目:初中化学 来源: 题型:选择题
| A. | 碧碧做完实验后,将剩余的金属和溶液回收 | |
| B. | 爽爽用点滴板代替试管,进行酸与指示剂反应 | |
| C. | 敏敏用高锰酸钾制氧气时,先点燃酒精灯,再去组装仪器 | |
| D. | 灵灵将配好的氯化钠溶液装入试剂瓶盖好瓶塞,贴标签备用 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
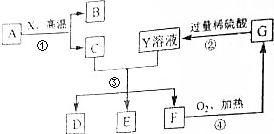
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 只有水能作溶液中的溶剂 | |
| B. | 由氢、氧两种元素组成的物质只有水 | |
| C. | 自然界中的水经沉淀、过滤、吸附、杀菌后可得到纯净的水 | |
| D. | 水可以灭火,主要利用了降低温度到可燃物着火点以下的原理 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
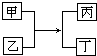
| A. | 若甲是稀盐酸,则乙可能是四种不同类别的物质 | |
| B. | 若甲是澄清的石灰水,则生成物中一定有沉淀 | |
| C. | 若丁为水,则反应物中一定有酸或碱 | |
| D. | 若丁为铜,则该反应一定是置换反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
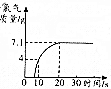 实验室用足量二氧化锰与浓盐酸加热制取氯气,当反应时氯化锰与氯化氢混合溶液中氯化氢的质量分数降低至20%,反应停止.反应方程式为:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+2H2O+Cl2↑.
实验室用足量二氧化锰与浓盐酸加热制取氯气,当反应时氯化锰与氯化氢混合溶液中氯化氢的质量分数降低至20%,反应停止.反应方程式为:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+2H2O+Cl2↑.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com