
【题目】下图是二氧化碳的部分知识网络图(反应条件已略)。
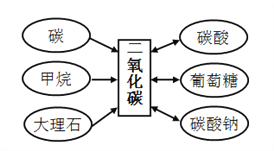
(1)保持二氧化碳化学性质的微粒是_________。
(2)甲烷中元素质量分数较小的是_________ 元素。
(3)葡萄糖(C6H12O6)________(填“是”或“不是”)有机物。
(4)碳酸(H2CO3)中C元素的化合价为_________。
科目:初中化学 来源: 题型:
【题目】在NaOH和Na2CO3的混合物9.3g中加入一定量的10.0%的稀盐酸,恰好完全反应, 将生成的气体全部通入足量的澄清石灰水中,产生5.0g沉淀。下列说法正确的是( )
A. 题中的一定量是7.3g
B. 反应共产生11.7gNaCl
C. 如用10%的稀盐酸将5.0g沉淀溶解,则所用稀盐酸的量与题中的一定量相等
D. Na2CO3消耗的稀盐酸比NaOH消耗的稀盐酸多
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】可用带柄V形玻璃管完成以下实验:

(1)如图1所示,往A处注入H2O2溶液,在B处下方加热使硫粉燃烧,产生的气体通入C处后排放的目的是 ,写出A处反应的化学方程式 ;
(2)如图2所示,A处盛浓氨水,B处放滴有无色酚酞试液的长滤纸条,可观察到的现象是 ,若另取一相同V形玻璃管(含相同的实验用品),在A处稍加热,在更短的时间内可观察到上述现象,请从微观角度解释 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】“H茶”为芝士(奶酪,是一种发酵的牛奶制品)现泡茶的原创者。自创立以来,受到年轻人欢迎,让我国饮茶这一古老文化焕发出新的生命力。下列说法正确的是

A. 芝士的主要成分是蛋白质,蛋白质属于有机高分子化合物
B. 配制该饮料的橙子富含维生素C,缺乏该物质会引起夜盲症
C. 上图中塑料袋加热熔化,具有热固性
D. 茶叶中茶多酚化学式为C17H19N3O,该物质为无机物
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室部分装置如下图所示,回答下列问题。
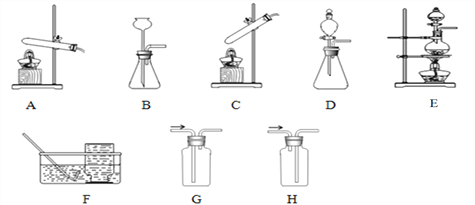
(1)实验室制取气体通过反应物状态,反应条件等选用相应的发生装置,根据气体的性质等选用相应的收集装置,请完成下表空格。发生装置、收集装置填字母。
气体 | 反应物、反应条件 | 化学方程式 | 发生装置 | 收集装置 |
O2 | 氯酸钾、二氧化锰固体、加热 | _____________ | 收集纯净的氧气用_______ | |
CO2 | 稀盐酸和大理石、常温 | _____________ | B或_______ | 收集干燥的二氧化碳用____________ |
Cl2 | 浓盐酸和二氧化锰固体、加热 | _____________ |
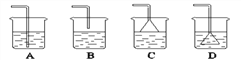
(2)氯气(Cl2)是有强烈刺激性气味的剧毒气体,能溶于水,与水反应生成______性物质,实验室用氢氧化钠溶液吸收尾气以免污染环境。为防止倒吸,选择______(下图,填字母,单选题)作为吸收氯气尾气的装置。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】“低钠盐”可以控制钠的摄入量从而防治高血压等疾病。制备“低钠盐”是在食盐中用NaCl按照配方比例添加食用KCl。国内某些生产厂家为改变“低钠盐”口味还会加入少量镁盐(仅限MgSO4或MgCl2)。
(1)测得某“低钠盐”样品a中只含有NaCl和KCl,该样品中的NaCl和KCl溶于
水时解离出的阴离子都是___________(填离子符号)。
(2)探究某“低钠盐”样品b中是否添加有镁盐,以及添加的是何种镁盐?
【猜想】I、不含镁盐 Ⅱ、含有硫酸镁 Ⅲ、含有氯化镁

【进行实验】
(3)请完成下表(已知BaSO4是难溶于水和酸的白色固体):
假设和现象 | 判断和化学方程式 | |
① | 若现象a为白色沉淀 | 则猜想____不成立。 |
② | 若现象a为_________, 现象b为_________。 | 则猜想Ⅲ成立。写出无色溶液B与硝酸中和反 应的化学方程式_________________。 |
③ | 若现象a、b均 为:产生白色沉淀 | 则猜想____成立。写出无色溶液B与硝酸钡溶液 反应的化学方程式______________。 |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小明同学用下图所示装置进行实验。甲瓶中充满二氧化碳气体,注射器中装有氢氧化钠浓溶液,乙中盛有足量稀盐酸。小明先关闭止水夹,然后将氢氧化钠浓溶液全部注入甲瓶,一段时间后再打开止水夹。
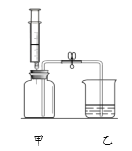
(1)注入氢氧化钠浓溶液后,甲中发生反应的化学方程式为_____________。
(2)打开止水夹,可观察到的现象有_____________、_____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学反应速率是衡量化学反应进行快慢的物理量,为了探究影响化学反应速率的因素,以过氧化氢分解为研究对象进行实验。各小组均可采用如图装置进行实验,记录收集10mL氧气的时间,实验室可供选择的试剂有:2.5%、5%、10%三种浓度的H2O2溶液、MnO2、CuO、红砖粉末。

A组:探究催化剂对化学反应速率的影响;
取5mL10%H2O2溶液,三次实验分别加人0.5gMnO2、红砖粉末、CuO进行实验,记录数据如下:
试剂 | MnO2 | 红砖粉末 | CuO |
t/s | 10 | 60 | 20 |
由此得出结论:MnO2、CuO对H2O2分解有催化作用,红砖粉末无催化作用。
(1)你认为该结论是否正确,为什么?_________________________________________。
(2)经过补充对比实验,证明红砖粉末有催化作用,则三者的催化效率由高到低的顺序为___________。
B组:探究浓度对化学反应速率的影响
甲同学:取10mL5%H2O2溶液,加入0.5gMnO2为催化剂,,进行实验,记录时间t1。
(3)乙同学:取10mL2.5%H2O2溶液,加入__________为催化剂,进行实验,记录时间t2。
实验结果:_______________________________________________________
结论:___________________________________________________________
【拓展探究】
(4)C组:探究____________对化学反应速率的影响。
各取10mL5%H2O2溶液和0.5gCuO为催化剂进行实验,两次实验分别将试管置于冰水浴和50℃热水浴,记录时间t3、t4。
(5)实验结果:_________________________;
结论:当反应物浓度和催化剂相同时,__________________________________。
(6)以上三组实验说明,影响化学反应速率的因素有:________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】水和溶液在生产、生活中有着重要的作用。
(1) 下列物质在水中不能形成溶液的是___________(填序号)。
A.白糖 B.汽油 C.食盐 D.高锰酸钾
(2) 甲、乙、丙三种固体物质在水中的溶解度曲线如图所示。
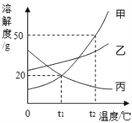
①随温度升高,溶解度减小的物质是_______________。
②t1℃时,分别向100g水中加入20g甲和20g乙,能形成饱和溶液的是__________。
③下列有关叙述正确的是__________(填序号)。
A.t2℃时,甲的饱和溶液中溶质的质量分数为50%
B.分别将甲和乙的饱和溶液从t2℃降到t1℃时,析出固体的质量为甲>乙
C.从接近饱和的甲溶液中析出一定量的甲晶体后,剩余溶液的溶质质量分数变小
D.t2℃时,分别将50g甲、乙、丙固体溶于水,配成饱和溶液,需要水的质量为甲<乙<丙
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com