
用锌与同一种硫酸溶液反应的五次实验结果记录如下:
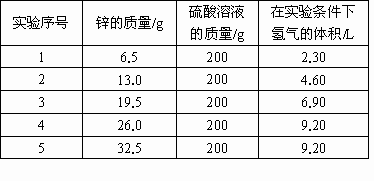
(1)哪一次实验是恰好完全反应的量?简述理由.
(2)求硫酸溶液中H2SO4的质量分数.
 新思维寒假作业系列答案
新思维寒假作业系列答案科目:初中化学 来源: 题型:
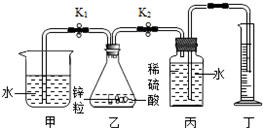
 (2012?常州)某研究性学习小组利用如图所示实验装置进行了以下探究实验.步骤如下:
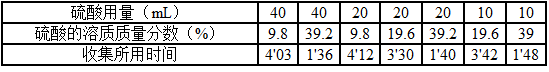
(2012?常州)某研究性学习小组利用如图所示实验装置进行了以下探究实验.步骤如下:| 硫酸用量(mL) | 40 | 40 | 20 | 20 | 20 | 10 | 10 |
| 硫酸的溶质质量分数(%) | 9.8 | 39.2 | 9.8 | 19.6 | 39.2 | 19.6 | 39.2 |
| 收集所用时间 | 4′03 | 1′36 | 4′12 | 3′30 | 1′40 | 3′42 | 1′48 |
查看答案和解析>>
科目:初中化学 来源:江苏中考真题 题型:实验题
查看答案和解析>>
科目:初中化学 来源: 题型:
研究性学习小组利用如图所示实验装置进行了以下探究实验.步骤如下:
①检查装置气密性,加入锌粒和稀硫酸;
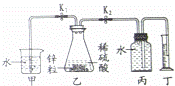 ②关闭K2、打开K1,待气泡连续均匀产生,立即关闭K1、打开K2,并开始计时;
②关闭K2、打开K1,待气泡连续均匀产生,立即关闭K1、打开K2,并开始计时;
③待丁中收集到10mL水,结束计时;
④换不同溶质质量分数、不同体积的稀硫酸,与质量相同的同一种锌粒重复上述实验;
⑤将每次实验的数据记录于下表:
| 硫酸用量(mL) | 40 | 40 | 20 | 20 | 20 | 10 | 10 |
| 硫酸的溶质质量分数(%) | 9.8 | 39.2 | 9.8 | 19.6 | 39.2 | 19.6 | 39.2 |
| 收集所用时间 | 4′03 | 1′36 | 4′12 | 3′30 | 1′40 | 3′42 | 1′48 |
(1)写出乙中反应的化学方程式: ;
(2)该实验的目的是:
(3)上述实验证明: 对该反应中氢气产生的速率有显著影响;
(4)若要快速制取大量氢气,可在乙中加入几滴硫酸铜溶液,但加入的量不可过多,原因是: (用化学方程式表示).
查看答案和解析>>
科目:初中化学 来源:2012年江苏省常州市中考化学试卷(解析版) 题型:填空题
| 硫酸用量(mL) | 40 | 40 | 20 | 20 | 20 | 10 | 10 |
| 硫酸的溶质质量分数(%) | 9.8 | 39.2 | 9.8 | 19.6 | 39.2 | 19.6 | 39.2 |
| 收集所用时间 | 4′03 | 1′36 | 4′12 | 3′30 | 1′40 | 3′42 | 1′48 |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com