

分析 (1)从锌和稀硫酸制取氢气,生成氢气密度密度比空气小;浓硫酸具有吸水性分析解答;
(2)①由于混合有空气或氧气的气体点燃时可能发生爆炸,去分析解答;
②氢气和氧化铜(黑色)发生反应生成红色的铜和水去分析解答;
③反应前后B2装置质量增加了1.8g说明反应后生成了1.8g水,去分析解答;
④如果没有连接B1,会使氢气中的水分也进入,使水分的质量偏大去分析解答.
解答 解(1)小明同学要收集一瓶干燥、纯净的氢气,浓硫酸除去水蒸气,最后用向下排空气法收集,所以仪器的连接顺序为:ABD;以锌和稀硫酸制取氢气,生成氢气的同时还生成硫酸锌,其化学方程式为:Zn+H2SO4=ZnSO4+H2↑
故答案为:ABD、Zn+H2SO4=ZnSO4+H2↑;
(2)①由于混合有空气或氧气的气体点燃时可能发生爆炸,因此点燃氢气前要检验氢气的纯度;
故答案为:检验氢气的纯度;
②装置B的作用为 除去氢气中的水蒸气,氢气和氧化铜(黑色)发生反应生成红色的铜和水,所以看到的现象是:黑色固体变为红色;
故答案为:除去氢气中的水蒸气;黑色固体变为红色;
③反应前后B2装置质量增加了1.8g说明反应后生成了1.8g水,
设生成1.8g水反应的氧化铜的质量为X
H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O
80 18
x 1.8g
$\frac{80}{18}$=$\frac{x}{18g}$
解之得:X=8g
所以氧化铜的质量分数为:8g÷9g=88.9%,故答案为:88.9%;
④实验结束后,小明发现装置中G中玻璃管内仍然有少量黑色固体,说明氧化铜没有完全反应,则小明③中计算出的该样品中CuO的质量分数 偏小.
故答案为:偏小
点评 注意在除去气体中的水分时,一定在最后一步除去,防止在除去其他气体的过程中又加入水分.


 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案科目:初中化学 来源:2017届内蒙古牙克石市九年级5月毕业生学业水平模拟测试化学试卷(解析版) 题型:选择填充题
下列有关叙述中,正确的是
A. 20℃时,100g水中能溶解36gNaCl,所以20℃时NaCl的溶解度是36g
B. NaCl饱和溶液中加入大量水后,溶液中溶质的质量减少了
C. 饱和溶液降温后,都有溶质结晶析出
D. 溶液中各部分的密度相同
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
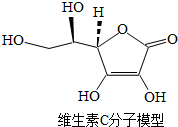 维生素C(化学式为C6H8O6)是人体必须的营养物质,能提高免疫力,预防癌症,保护牙龈等.下列有关维生素C的说法正确的是( )
维生素C(化学式为C6H8O6)是人体必须的营养物质,能提高免疫力,预防癌症,保护牙龈等.下列有关维生素C的说法正确的是( )| A. | 维生素C属于氧化物 | |
| B. | 维生素C中碳、氢、氧元素的质量比为3:4:3 | |
| C. | 维生素C分子中质子数和电子数一定相等 | |
| D. | 维生素C由碳、氢、氧三种原子构成 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 “人工智能”正逐步进入汽车制造领域,无人驾驶主要依靠车内的智能驾驶系统来实现.
“人工智能”正逐步进入汽车制造领域,无人驾驶主要依靠车内的智能驾驶系统来实现.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | H2SiO4 | B. | SiO2 | C. | Si | D. | SiH4 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

| 操作 | 现象 | 解释或结论 |
| ①取少量固体于试管中,加适量水振荡,用手触摸 试管外壁;静置,滴入 几滴无色酚酞试液 | 试管外壁发烫; 酚酞试液变红色. | 说明剩余固体中含有氧化钙.氧化钙 溶于水生成氢氧化钙,同时放出(填“放出”或“吸收”)热量. |
| ②再取少量固体于另一 试管中滴加过量稀盐酸 | 试管中有气泡产生 | 说明剩余固体中含有碳酸钙. |
| 时间 | 称量项目 | 质量/g |
| 反应开始前 | 装置+稀盐酸+试样 | 171.0 |
| 反应结束后 | 装置+稀盐酸+试样 | 166.6 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com