
【题目】请根据下列装置,回答问题:
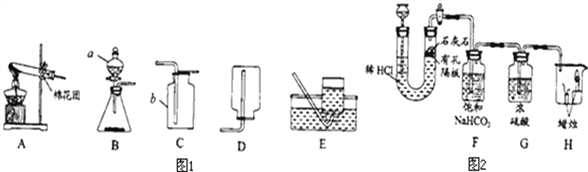
(1)写出图1中有标号仪器的名称: b______.
(2)①用高锰酸钾制取一瓶氧气,可选用装置A和______(选填序号)组合.装入药品前要先______;实验所用高锰酸钾工业上可用高纯度的二氧化锰为原料制取,主要流程如下:
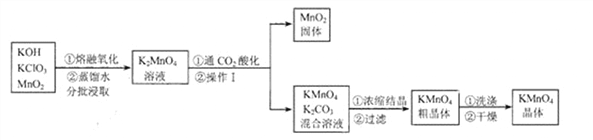
已知相关物质的溶解度(20℃)如下表:

②流程里K2MnO4中锰元素的化合价为__________。
③操作I的名称是_____。“干燥”过程中温度不宜过高的原因是_________________(用化学方程式表示)。
④“通CO2酸化”,反应的化学方程式为: 3K2MnO4+2CO2=2KMnO4+MnO2↓+2K2CO3 若用稀H2SO4酸化,反应的化学方程式为: 3K2MnO4+2H2SO4=2KMnO4 +MnO2↓+2K2SO4+2H2O 工业上不采用稀H2SO4酸化的原因是____________________。
⑤电解法也可以实现由K2MnO4向KMnO4的转化,反应的化学方程式为:![]() 与“通CO2酸化”相比,其优点是___________。
与“通CO2酸化”相比,其优点是___________。
(3)用双氧水和二氧化锰制氧气,二氧化锰的作用是____,可选用的发生装置是____(填序号)。
(4)用如图2装置制取CO2并验证相关性质。
①生成CO2反应的化学方程式_________,该反应属_______反应(写基本反应类型);
②F装置的作用是______;
③H装置中的现象可说明CO2具有的性质是______(答一点即可)。
【答案】 集气瓶 C 或 E 检查装置气密性 +6 过滤 2KMnO4![]() K2MnO4+MnO2+O2↑ 相同条件下硫酸钾和高锰酸钾溶解度都比较小无法采用浓缩结晶的方法分离 生成的氢氧化钾可以循环使用、转化率高没有锰元素损失或锰元素利用率高 催化作用 B CaCO3+2HCl=CaCl2+H2O+CO2↑ 复分解反应 吸除二氧化碳中的氯化氢气体 二氧化碳不能燃烧、不能支持燃烧、密度比空气大
K2MnO4+MnO2+O2↑ 相同条件下硫酸钾和高锰酸钾溶解度都比较小无法采用浓缩结晶的方法分离 生成的氢氧化钾可以循环使用、转化率高没有锰元素损失或锰元素利用率高 催化作用 B CaCO3+2HCl=CaCl2+H2O+CO2↑ 复分解反应 吸除二氧化碳中的氯化氢气体 二氧化碳不能燃烧、不能支持燃烧、密度比空气大
【解析】(1)图1中有标号仪器的名称: b:集气瓶;(2)①氧气的密度比空气大,可用向上排空气法收集,选择装置C;氧气难溶于水,也可以选择排水集气法的装置E,所以用高锰酸钾制取一瓶氧气,可选用装置A和C 或 E组合.装入药品前要先检查装置气密性;②化合物中元素的化合价代数和为零,钾元素显+1价,氧元素显-2价,K2MnO4中锰元素的化合价为+6;③操作I的目的是将难溶性固体与液体分离,名称是过滤。“干燥”过程中温度不宜过高的原因是高锰酸钾加热条件下会分解,反应方程式为:2KMnO4![]() K2MnO4+MnO2+O2↑;④由题中信息可知,用硫酸酸化会生成硫酸钾,相同条件下硫酸钾和高锰酸钾溶解度都比较小无法采用浓缩结晶的方法分离,故工业上不采用稀H2SO4酸化; ⑤由题中信息可知,电解法生成的氢氧化钾可以循环使用、转化率高、没有锰元素损失或锰元素利用率高 (3)用双氧水和二氧化锰制氧气,二氧化锰的作用是催化作用(或加快过氧化氢分解速率),可选用的发生装置是固液常温型B;(4)①石灰石的主要成分是碳酸钙,和稀盐酸反应生成二氧化碳、氯化钙和水,反应的化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑,该反应属复分解反应;②盐酸有挥发性,挥发出来的氯化氢气体混在二氧化碳中,导致收集二氧化碳不纯,碳酸氢钠和盐酸反应生成二氧化碳,所以F装置的作用是吸除二氧化碳中的氯化氢气体;③H装置中的现象是蜡烛由低到高依次熄灭,可说明CO2具有的性质是二氧化碳不能燃烧、不支持燃烧、密度比空气大。
K2MnO4+MnO2+O2↑;④由题中信息可知,用硫酸酸化会生成硫酸钾,相同条件下硫酸钾和高锰酸钾溶解度都比较小无法采用浓缩结晶的方法分离,故工业上不采用稀H2SO4酸化; ⑤由题中信息可知,电解法生成的氢氧化钾可以循环使用、转化率高、没有锰元素损失或锰元素利用率高 (3)用双氧水和二氧化锰制氧气,二氧化锰的作用是催化作用(或加快过氧化氢分解速率),可选用的发生装置是固液常温型B;(4)①石灰石的主要成分是碳酸钙,和稀盐酸反应生成二氧化碳、氯化钙和水,反应的化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑,该反应属复分解反应;②盐酸有挥发性,挥发出来的氯化氢气体混在二氧化碳中,导致收集二氧化碳不纯,碳酸氢钠和盐酸反应生成二氧化碳,所以F装置的作用是吸除二氧化碳中的氯化氢气体;③H装置中的现象是蜡烛由低到高依次熄灭,可说明CO2具有的性质是二氧化碳不能燃烧、不支持燃烧、密度比空气大。


科目:初中化学 来源: 题型:
【题目】现代工业常以氯化钠为原料制备纯碱,部分工艺流程如下:

(1)已知20℃,氧化钠溶解度为36g,则20时饱和食盐水溶质质量分数为______________;(保留1位小数)
(2)反应①的化学方程式是_______________________;
(3)甲溶液中能与石灰乳反应生成氨气的物质是_____________,实验室中通常检验氨气的试剂是______________;
(4)反应②的化学方程式是_____________________;
(5)整个生产过程中可循环利用的物质是_________________;
(6)为测定产品纯碱中钠元素质量分数,取样(样品中除纯碱外还含有碳酸氢钠和少量不溶性杂质)设计如下实验过程:
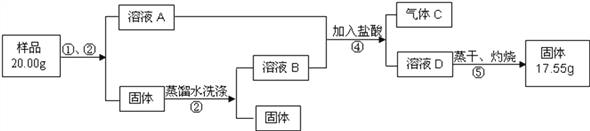
请回答:
Ⅰ.操作①是溶解,操作②为__________________;
Ⅱ.原样品中钠元素的质量分数为___________________;
Ⅲ.若测定结果偏低,原因可能是__________(填字母)。
A.溶液D中含有Na2CO3 B.溶液D中含有NaCl
C.操作③中固体没有洗涤干净 D.操作④中加入过量的盐酸
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是甲、乙、丙三种固体物质的溶解度曲线,且它们溶于水时溶液温度均无明显变化。
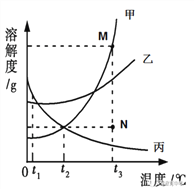
(1)t3℃时,N点的丙溶液为________溶液(饱和或不饱和)
(2)t2℃时,等质量的甲、乙两种物质的饱和溶液中溶剂的质量大小关系为甲________乙(填“>”、“<”或“=”)。
(3)t3℃时,若要将N点的甲溶液转变为M点的甲溶液,可以采用的方法是_____________________;__________________。
(4)t3℃时,M点对应的溶解度为50g,此点甲溶液的质量分数是________(保留一位小数)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下图从A或B两题中任选一个作答,若两题均作答,按A计分。
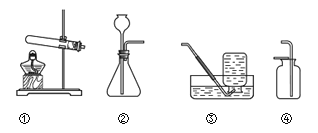
A | B |
(1)选用装置①制氧气的化学方程式为____________。 (2)选用装置③收集氧气的理由为____________。 | (1)选用装置②制二氧化碳的化学方程式为___________。 (2)选用装置④收集二氧化碳时,检验气体是否集满的操作是___________。 |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】右图是A、B、C三种物质的溶解度曲线。下列叙述正确的是 ( )
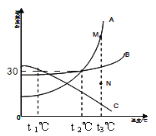
A.t1℃时三种物质的饱和溶液升温到t3℃所得溶液溶质质量分数大小关系为A>B>C
B.t2℃时,A、B两种物质的溶液中所含溶质质量相等
C.t2℃时,20g B溶解于50g水中能形成70溶液
D.若要将组成在N点的A溶液转变为M点的A溶液,可以采取恒温蒸发溶剂的方法
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】CO2是中学化学中常见的气体,请根据下列装置图回答问题:
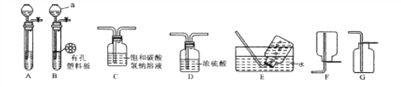
(1)仪器a的名称是_________;实验室制取CO2时,选用B装置比选用A装置的好处是____________;实验室还可用B装置制取的气体有____________等(需体现出该装置的优点)
(2)稀盐酸能挥发出HCl气体,因此需要用饱和 NaHCO3溶液除去CO2中的HCl,用化学方程式表示其原理____________;收集CO2应选用的装置是_________(填对应装置的序号)
(3)已知将CO2通入紫色石蕊试液中,溶液会变红,原因是_______________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学用语是学习化学的重要工具
(1)按要求写出相应的化学符号
①碳原子_____②空气中最多的气体_______③锌离子______④两个碳酸根离子______
⑤缺少后会导致骨质疏松的元素_________⑥“西气东输”中的“气”是_______
(2)按要求写出相应的化学方程式,并注明反应的基本类型
①铝在空气中形成致密的保护膜________________________,反应类型____________
②用氢氧化镁治疗胃酸过多_______________________,反应类型____________
③水在通电条件下分解________________________,反应类型____________
④用锌与稀硫酸反应制取氢气________________________,反应类型____________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】阅读下面科普短文(本文由网络文章改写)。
松花蛋又称皮蛋、变蛋、灰包蛋等,因剥开蛋壳后胶冻状的蛋清中常有松针状的结晶或花纹而得名,是一种我国传统风味食品,口感鲜滑爽口,色香味均有独到之处。中医认为,松花蛋性凉,对牙痛、眼痛等疾病有一定疗效。由于松花蛋会有一股碱涩味,在吃松花蛋的时候可以加入少量的姜醋汁。
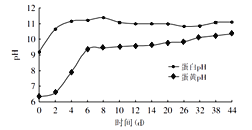
松花蛋是用料泥包裹鸭蛋、鸡蛋等加工而成。料泥是由生石灰、纯碱、食盐、红茶、草木灰(主要成分K2CO3)等原料与水按比例混合均匀制得。料泥制作过程中,通过一系列反应,产生的强碱(NaOH、KOH)经蛋壳渗入到蛋清和蛋黄中,与其中的蛋白质作用,致使蛋白质分解、凝固并放出少量硫化氢气体和氨气。同时渗入的碱还会与蛋白质分解出的氨基酸进一步发生中和反应,生成的盐的晶体沉积在凝胶态的蛋清中,便出现了朵朵“松花”。而硫化氢气体则与蛋清和蛋黄中的矿物质作用生成各种硫化物,使蛋清和蛋黄的颜色发生改变,蛋清呈特殊的茶褐色、蛋黄则呈墨绿色。下图表示松花蛋腌制时间与其中蛋清和蛋黄的pH的变化关系。
很多人在平时生活中都非常喜欢吃皮蛋瘦肉粥、凉拌松花蛋,专家提醒这种食物少吃无妨,却不能过多食用。其一,松花蛋腌制过程中蛋白质分解、变质,导致营养价值遭到了一定的破坏。其二,市售松花蛋还可能含铅(国家规定松花蛋中铅含量需小于0.5mg/kg)。微量铅很容易被儿童吸收,导致铅中毒。其三,剥开皮的松花蛋1至2小时内一定要吃完,若长时间暴露在空气中,非常容易感染沙门氏杆菌,沙门氏杆菌会快速繁殖,此时食用松花蛋很容易引起中毒现象,依据文章内容,回答下列问题。
(1)食用松花蛋时加入少量姜醋汁可以除去松花蛋中________味。
(2)料泥制作过程中会生成强碱NaOH和KOH,钾元素来自于原料中的________。请写出Na2CO3与Ca(OH)2反应的化学方程式为________。
(3)依据松花蛋腌制时间与其中蛋清和蛋黄pH的变化关系判断,当蛋清和蛋黄pH均达到9以上时,松花蛋至少腌制的天数为________(填字母序号,下同)。
A.2天 B.6天 C.12天 D.32天
(4)下列关于松花蛋的说法正确的是________。
A.松花蛋特殊颜色的形成与硫化氢气体有关
B.松花蛋具有很高的营养价值,成人可以多吃
C.市售松花蛋可能含有少量的铅,儿童不宜食用
D.剥开皮的松花蛋隔夜放置后依然可以放心食用
查看答案和解析>>
科目:初中化学 来源: 题型:
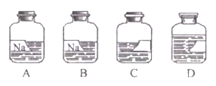
【题目】某化学课外小组的同学,在实验室发现四瓶标签破损的无色溶液(如下图所示),其中A、B试剂瓶标签部分破损,C、D试剂瓶标签完全破损。根据查阅药品记录表可知,A、B、C、D分别是NaOH溶液、Na2CO3溶液、石灰水、CaCl2溶液中的一种。
在老师的指导下,化学课外小组同学进行了下述实验。
老师给准备的试剂有:稀盐酸、NaHCO3溶液和酚酞溶液。
(1)分别取A、B、C、D溶液于4支试管中,向其中分别滴加酚酞溶液,发现A、B、C溶液变红,说明这3种溶液呈__________ (填“酸性”、“碱性”或“中性”)。由该实验可确定的溶液为___________ (填试剂瓶序号及相应的溶液名称)。
(2)分别取A、B溶液于两支试管中,加入足量的稀盐酸,发现均有气泡产生,小组同学利用上述共计7种试剂,经过下述实验最终确定了这两份溶液的成分。
实验操作 | 现象 | 实验结论 |
①分别取A、B溶液于2支试管中,向其中分别滴加_________; ②过滤后,分别向滤液中滴加______。 | 白色沉淀 A:___________ B:___________ | A是Na2CO3溶液; B是变质的NaOH溶液 |
写出B溶液中加入足量的稀盐酸发生反应的化学方程式 ___________________。
(3)取C溶液于试管中,逐滴加入一定量的NaHCO3溶液,充分反应,观察到溶液变浑浊,过滤,滤液中除了H外,还含有较大量的阳离子是_________(填离子符号)查阅资料可知:Ca(OH)2+NaHCO3=CaCO3↓+NaOH+H2O、NaOH+ NaHCO3=Na2CO3+H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com