
【题目】氧化铝(Al2O3)、氮化铝(AlN)都是一种重要的无机非金属材料,广泛应用于矿业生产和集成电路生产领域,某化学课题小组的同学在实验室里进行氮化铝的制备并测定其含量的实验。
【实验一】制备氮化铝
【资料1】实验室常用饱和亚硝酸钠与氯化铵溶液反应制取纯净的氮气。
有关反应的化学方程式为:
NaNO2+NH4Cl NaCl+N2↑+2H2O(此反应是放热反应);
Al2O3+3C+N2![]() 2AlN+3CO
2AlN+3CO
试回答:
(1)氮化铝(AlN)中氮元素的化合价是。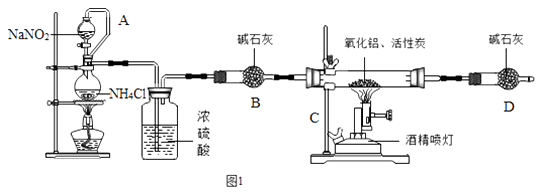
(2)加入药品前必须进行的一个实验步骤是 , 加热片刻后即可移去酒精灯,不需继续加热,其理由是。上述实验装置中存在一些不足,请指出。
(3)在制取氮化铝时由于反应不完全,所得氮化铝产品中的杂质除氧化铝之外,还可能含有(填化学式)。
(4)【实验二】氮化铝含量测定
【资料2】有关氮化铝(AlN)、氧化铝和偏铝酸钠(NaAlO2)的相关反应的化学方程式为:
①AlN+NaOH+H2O=NaAlO2+NH3↑
②Al2O3 + 2NaOH= 2NaAlO2 + H2O
③2NaAlO2 + CO2 + 3H2O = 2Al(OH)3↓ + Na2CO3
【定性分析】
步骤一:小红取C装置中少量固体样品于试管中,加足量氢氧化钠溶液,固体逐渐消失,并得到无色溶液,试管口闻到有刺激性气味的气体生成,则该样品中含有氮化铝。
步骤二:小亮继续在上述无色溶液中通人二氧化碳气体出现白色沉淀,于是他认为样品中一定还存在氧化铝。你认为小亮的结论是否正确,理由是。
(5)【定量测定】.
【资料3】氨气的溶解性:极易溶于水,但难溶于有机溶剂四氯化碳(CCl4)和碱性溶液等。
图2装置通过测量氨气的体积从而测定氮化铝的含量。
小燕同学进行如下操作:(a)往广口瓶中放入适量的氮化铝样品;(b)打开分液漏斗的活塞往锥形瓶中加入过量的浓NaOH溶液;(c)检验装置气密性;(d)测定收集到X液体的体积。
正确的操作顺序为(用a、b、c、d字母表示)。
(6)图2中X液体可能为。
A.水
B.四氯化碳
C.氢氧化钠溶液
(7)图3装置则是通过测定吸收氨气的质量从而测定氮化铝的含量。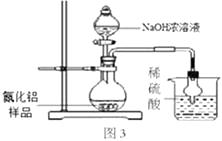
小萍同学进行了如下操作:取氮化铝样品10.0克进行实验,实验结束后烧杯中物质增重3.4克,请你帮小萍同学计算,她取用的样品中氮化铝的质量分数是多少?
(8)图3所示方案会导致该样品中氮化铝含量测定结果偏低,为提高测定结果的精确度,在不改动装置的前提下,可采取的措施是。
【答案】
(1)-3
(2)检查装置气密性,该反应是放热反应,没有尾气处理装置
(3)C
(4)因为氮化铝与氢氧化钠溶液反应生成偏铝酸钠,再与二氧化碳和水反应生成氢氧化铝沉淀,所以样品中不一定有氧化铝
(5)cabd
(6)B,C
(7)82%;
(8)待反应结束后,从分液漏斗中通入足量的氢氧化钠溶液使残留在装置内的气体完全被稀硫酸吸收
【解析】:(1)化合价代数和为零,氮化铝(AlN)中铝元素显示+3价,所以氮元素的化合价是-3;
(2)加入药品前必须进行的操作是检查装置的气密性;饱和亚硝酸钠与氯化铵溶液反应放出热量;一氧化碳有毒不能直接排放,需要尾气处理;
(3)反应物中碳和氧化铝是固体,可能混入产物中,所以氮化铝产品中的杂质除氧化铝之外,还可能含有C;
(4)偏铝酸钠、二氧化碳和水反应生成氢氧化铝和碳酸钠,所以小亮的结论不正确;
(5)实验时,应该先检验装置的气密性,然后再加入药品,所以正确的操作顺序为:cabd;
(6)广口瓶中的试剂X的作用是将氨气与水隔开,因为氨气极易溶于水,要用四氯化碳将氨气与水隔开,水不溶于四氯化碳,故选:B;
(7)烧杯中物质增重3.4克,就是生成的氨气的质量,
设样品中AlN的质量为x
AlN+NaOH+H2O=NaAlO2+NH3↑
41 17
x 3.4g![]() =
=![]()
x=8.2g
所以样品中AlN的质量分数为:![]() ×100%=82%;
×100%=82%;
(8)装置测得的结果偏低是因为生成的氨气会残留在集气瓶内,导致不能被硫酸充分吸收.讲稀硫酸换成浓硫酸一方面没有意义,另一方面还会导致浓硫酸吸收空气中的水蒸气使得测量结果偏大,可采取的措施是:反应结束后,向烧瓶内继续加入足量的氢氧化钠溶液,使装置内残留气体排出,被烧杯中的硫酸充分吸收.
所以答案是:(1)-3;(2)检验装置的气密性;该反应属于放热反应;没有尾气处理装置;(3)C;(4)不正确,偏铝酸钠和二氧化碳反应也会生成氢氧化铝沉淀;(5)cabd;(6)B;(7)82%;(8)反应结束后,向烧瓶内继续加入足量的氢氧化钠溶液,使装置内残留气体排出,被烧杯中的硫酸充分吸收.
【考点精析】解答此题的关键在于理解书写化学方程式、文字表达式、电离方程式的相关知识,掌握注意:a、配平 b、条件 c、箭号,以及对根据化学反应方程式的计算的理解,了解各物质间质量比=系数×相对分子质量之比.


 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案科目:初中化学 来源: 题型:
【题目】请用“左边”或“右边”填写下列空白. 两边同时加入金属后,哪边反应快? . 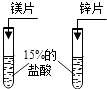
两边同时加入固体后,哪边试管璧热 .
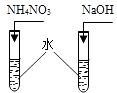
通电一段时间后,试管里哪边液面高 . 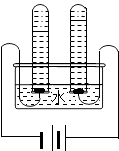
取下镁带点燃后,将生成物全部放回,哪边重? . 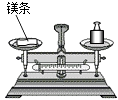
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我们在利用物质的某些性质时,可能有利于人类,也可能给人类带来危害.请你仿照示例,填写表:
物质 | 有利于人类的事例 | 不利于人类的事例 |
示例:氧气 | 氧气可以供给呼吸,用于潜水和医疗 | 食物易发生腐烂,食品应采用真空包装 |
(1)氮气 | ___ | ___ |
(2)二氧化碳 | ___ | ___ |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】分类法是化学学习的重要方法。下列有关分类中正确的是( )
A. 铁、锌、碘元素都是人体必需的微量元素
B. 煤、石油和甲烷都是不可再生的化石燃料
C. 熟石灰、烧碱和浓硫酸都可做干燥剂
D. 塑料、合金和合成纤维都属于合成材料
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】分类是学习和研究中一种常用的科学方法。下列物质中按照单质、酸、混合物的顺序排列的是( )
A. 白磷 硫酸 冰水混合物
B. 氢气 碳酸 空气
C. 石墨 二氧化碳 石油
D. 生铁 盐酸 粗盐
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列现象描述正确的是( )
A. 红磷在空气中燃烧产生大量白雾
B. 紫色石蕊溶液能使稀硫酸变红
C. 硫在空气中燃烧发出淡蓝色火焰
D. 光亮的铁丝浸入稀盐酸形成黄色溶液
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】取一定量的氧化铁与氧化铜的混合物,加入稀硫酸充分反应,消耗H2SO4共9.8g,原混合物中氧元素的质量是( )
A.0.8g
B.1.6g
C.3.2g
D.6.4g
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学就在我们身边,现有下列几种物质:①二氧化碳 ②水 ③稀硫酸 ④氢气,请用序号填空.
(1)常用作溶剂的是_____
(2)可用人工降雨的气体是_____
(3)最清洁的燃料是_____
(4)用于金属表面除锈的是_____
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com