
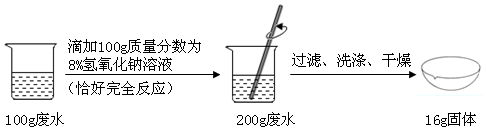
分析 根据氢氧化钠的质量结合对应的化学方程式求算生成的氯化钠的质量,进而结合最后的固体为16g求算原混合物中氯化钠的质量,最后求算其质量分数.
解答 解:设反应生成的氯化钠的质量为x
NaOH+HCl=NaCl+H2O
40 58.5
100g×8%=8g x
$\frac{40}{58.5}$=$\frac{8g}{x}$
x=11.7g
则原混合物中氯化钠的质量为16g-11.7g=4.3g
则废水中氯化钠的质量分数为$\frac{4.3g}{100g}$×100%=4.3%
答:(1)当恰好完全反应,生成氯化钠的质量为 11.7g.
(2)该种工业废水中氯化钠的质量分数为4.3%.
点评 根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整.


科目:初中化学 来源: 题型:选择题
| A. | 胶头滴管只能吸取一种药品 | |
| B. | 与滴瓶配套的胶头滴管使用后不必洗涤 | |
| C. | 吸液后的胶头滴管可以平放 | |
| D. | 为防止溅出,滴加液体时胶头滴管应伸入试管 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com