
| A. | 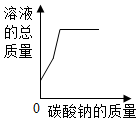 向稀盐酸中加入碳酸钠粉末 | |
| B. | 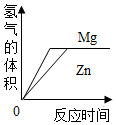 等质量足量的镁、锌分别和等质量等浓度的盐酸反应 | |
| C. | 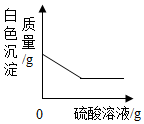 在碳酸钡中不断滴加硫酸溶液 | |
| D. | 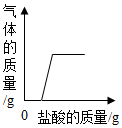 向氢氧化钠溶液中滴加盐酸,利用图象可知氢氧化钠已部分变质 |
分析 A、稀盐酸和碳酸钠反应生成氯化钠、水和二氧化碳;
B、镁比锌活泼,和盐酸反应时速率较快;
C、碳酸钡和稀硫酸反应生成硫酸钡沉淀、水和二氧化碳;
D、氢氧化钠能和二氧化碳反应生成碳酸钠和水,向碳酸钠和氢氧化钠共存的溶液中加入稀盐酸时,稀盐酸先和氢氧化钠反应生成氯化钠和水,后和碳酸钠反应生成氯化钠、水和二氧化碳.
解答 解:A、向稀盐酸中加入碳酸钠粉末时,稀盐酸和碳酸钠反应生成氯化钠、水和二氧化碳,溶液质量增大,同时碳酸钠溶于水时溶液质量增大,当稀盐酸完全反应后,碳酸钠溶解达到饱和状态时,溶液总质量不再变化,该选项对应关系正确;
B、等质量足量的镁、锌分别和等质量等浓度的盐酸反应时,由于镁比锌活泼,和盐酸反应时速率较快,反应需要的时间短,最终生成的氢气质量相等,该选项对应关系正确;
C、在碳酸钡中不断滴加硫酸溶液时,碳酸钡和稀硫酸反应生成硫酸钡沉淀、水和二氧化碳,随着反应进行,沉淀质量增大,该选项对应关系不正确;
D、向氢氧化钠溶液中滴加盐酸时,如果氢氧化钠没有变质,则不会产生气体,该选项对应关系正确.
故选:C.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.


 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案科目:初中化学 来源: 题型:选择题
| A. | LiMnO2是氧化物 | B. | 该反应是化合反应 | ||
| C. | 此反应中,二氧化锰是催化剂 | D. | LiMnO2中锰元素的化合价显+2价 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
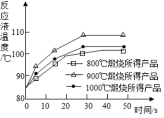
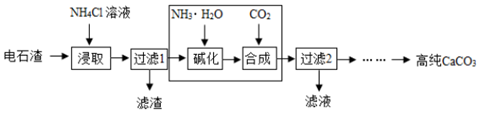
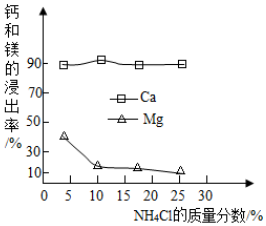
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
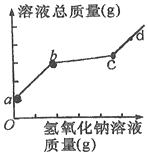 将某氢氧化钠溶液逐滴滴入盐酸和氯化铁的混合溶液中,直至过量.根据空验事实绘制如图所示曲线.其中说法正确的是( )
将某氢氧化钠溶液逐滴滴入盐酸和氯化铁的混合溶液中,直至过量.根据空验事实绘制如图所示曲线.其中说法正确的是( )| A. | ab段红褐色沉淀质量增加 | B. | bc段氯化钠质量不断减少 | ||
| C. | cd段溶液的pH不断减小 | D. | b点所含溶质种类比c点多 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
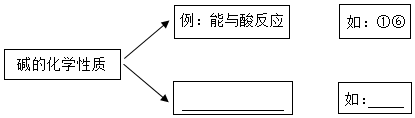 分类是学习化学常用的方法.
分类是学习化学常用的方法.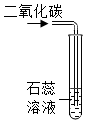 | 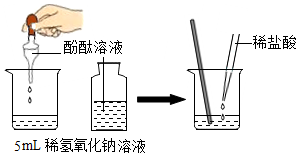 | 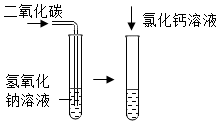 |
| A | B | C |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com