
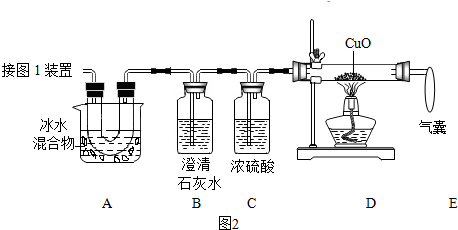
分析 根据碳酸钙难溶于水,硫酸铜在溶液中显蓝色,硫酸根离子、碳酸根离子与钡离子会生成白色的硫酸钡沉淀、碳酸钡沉淀,碳酸钡沉淀会溶于硝酸,硫酸钡沉淀不溶于硝酸,氯离子和银离子会生成氯化银沉淀,氯化银沉淀不溶于硝酸等知识进行分析.
解答 解:取少量样品溶于水得到无色溶液,所以杂质中一定不含硫酸铜、碳酸钙,然后滴加过量的氯化钡溶液,出现白色沉淀A,过滤,沉淀A中加入过量的稀硝酸,沉淀部分消失并放出气体,所以杂质中一定含有硫酸钾、碳酸钾,往步骤①所得的滤液中加入适量硝酸银溶液和稀硝酸,生成白色沉淀B,步骤①中加入的过量氯化钡,所以步骤①所得的滤液中含有氯离子,杂质中可能含有氯化钾,氯化钙和碳酸钾会生成白色沉淀,不能共存,所以杂质中一定不含:氯化钙.
(1)通过推导可知,步骤②中放出的气体是:二氧化碳;
(2)通过推导可知,白色沉淀B是氯化银,氯化钾和硝酸银反应生成氯化银沉淀和硝酸钾,化学方程式为:AgNO3+KCl=AgCl↓+KNO3;
(3)通过推导可知,杂质中一定含有硫酸钾、碳酸钾,一定没有碳酸钙、硫酸铜、氯化钙,可能含有氯化钾.
故答案为:(1)二氧化碳;
(2)氯化银,AgNO3+KCl=AgCl↓+KNO3;
(3)硫酸钾、碳酸钾,碳酸钙、硫酸铜、氯化钙,氯化钾.
点评 在解此类题时,首先分析题中所给物质的性质,然后依据题中的现象确定各种物质的存在性,最后确定混合物的成分.


科目:初中化学 来源: 题型:选择题
| A. | 熟石灰 | B. | 稀盐酸 | C. | 硫酸铜 | D. | 二氧化碳 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
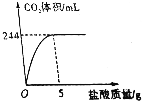 将20g稀盐酸加入到1.25g石灰石样品中反应,生成的CO2体积与加入盐酸质量的关系如图所示(已知本实验条件下CO2的密度为1.8g/L).
将20g稀盐酸加入到1.25g石灰石样品中反应,生成的CO2体积与加入盐酸质量的关系如图所示(已知本实验条件下CO2的密度为1.8g/L).查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 熔点 | 沸点 | 热稳定性 | 其他 |
| 101℃~102℃ | 150℃~160℃升华 | 100.1℃分解出水,175℃分解成CO2、CO、H2O | 与 Ca(OH)2反应产生白色沉淀(CaC2O4) |

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验一 | 实验二 | 实验三 | |
实验 方案 | 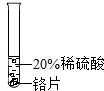 | 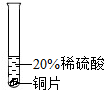 | 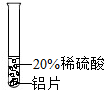 |
| 实验 现象 | 铬片表面产生气泡缓慢,溶液变蓝色. | 无明显实验现象 | 铝片表面产生气泡较快. |
| 结论 | 铬能和稀硫酸发生反应,反应速率较慢. | 铜不与稀硫酸反应 | 铝能与稀硫酸发生反应,反应速率较快 |
| 三种金属在金属活动性顺序中的相对位置关系是Al>Cr>Cu或AlCrCu | |||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com