
| 实验操作 | 实验现象 | 结论 | |
| 方案1 | 取样品少量于试管中,加入适量水,震荡,样品全部溶于水,向其中加入无色酚酞溶液 | 溶液变成 色 |
白色物质 为Na2O |
| 方案2 | ①取样品少量于试管中,加入适量水,震荡,样品全部溶于水,向其中加入过量的氯化钙溶液 | 出现白色沉淀 | 白色物质 是 |
| ②静置片刻,取上层清液于试管中,滴加无色酚酞溶液 | 无明显现象 |
| ||
| 实验操作 | 实验现象 | 结论 | |
| 方案1 | 取样品少量于试管中,加入适量水,震荡,样品全部溶于水,向其中加入无色酚酞溶液 | 溶液变成红 色 |
白色物质 为Na2O |
| 方案2 | ①取样品少量于试管中,加入适量水,震荡,样品全部溶于水,向其中加入过量的氯化钙溶液 | 出现白色沉淀 | 白色物质 是Na2CO3 |
| ||


 精英口算卡系列答案
精英口算卡系列答案科目:初中化学 来源: 题型:
| A、甲同学说,二氧化碳也能支持燃烧,所以它不能用于灭火 | ||||
| B、乙同学说,二氧化碳只能支持镁等少数活泼金属燃烧,因此,它不能用于活泼金属的灭火 | ||||
C、丙同学写出了镁在二氧化碳中燃烧的化学方程式:Mg+CO2
| ||||
| D、丁同学说,这个反应属于置换反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:
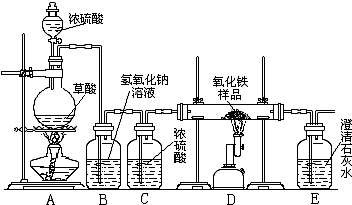
 某校化学课外兴趣小组的同学在研究性学习课上展示了一套如下图所示实验装置(假设每步化学反应都完全,氧化铁样品中的杂质不参加反应).查阅资料:草酸在浓硫酸存在时加热发生如下反应:H2C2O4
某校化学课外兴趣小组的同学在研究性学习课上展示了一套如下图所示实验装置(假设每步化学反应都完全,氧化铁样品中的杂质不参加反应).查阅资料:草酸在浓硫酸存在时加热发生如下反应:H2C2O4| 浓硫酸 | △ |
查看答案和解析>>
科目:初中化学 来源: 题型:
| ||
| △ |

| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| ||
| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
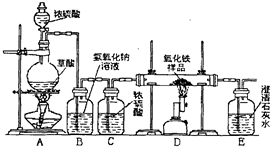 某校化学课外兴趣小组的同学在研究性学习课展示了一套如图所示的实验装置(假设每步化学反应都完全,氧化铁样品中的杂质不反应).查阅资料:草酸在浓硫酸存在时加热发生如下反应:
某校化学课外兴趣小组的同学在研究性学习课展示了一套如图所示的实验装置(假设每步化学反应都完全,氧化铁样品中的杂质不反应).查阅资料:草酸在浓硫酸存在时加热发生如下反应:
|
| ||
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com