
【题目】下列装置能完成相应实验的是( )

A. 装置①:过氧化氢制氧气B. 装置②:由B端进收集氧气
C. .装置③:氯酸钾制氧气D. 装置②:瓶内装水,由A端进气收集氧气
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:
【题目】我国古代将炉甘石(ZnCO3)、赤铜(Cu2O)和木炭粉混合后加热到约800℃,可以得到一种外观似金子的锌和铜的合金。小明同学在实验室按古代方法将炉甘石、赤铜和木炭粉混合加热一段时间,得到固体混合物A.固体混合物A的成分是什么?他对此进行了实验探究。
(查阅资料)①ZnCO3加热可分解为ZnO;②Cu2O+H2SO4═CuSO4+Cu+H2O
(实验探究)
步骤Ⅰ取混合物A适量于烧杯中,加入过量稀硫酸,充分反应后过滤,得到滤渣B和蓝色溶液C,同时生成了一种气体,将该气体通入澄清石灰水无明显现象;
步骤Ⅱ在滤渣B中加入足量硝酸银溶液,充分反应后过滤,得到银和蓝色溶液D。
(实验分析)
(1)炉甘石加热分解的化学方程式是_____;
(2)若向溶液C中加入过量的锌片,观察到的现象是_____;
(3)混合物A中一定含有_____(填化学式)。
(拓展延伸)
下列方法可用于鉴别锌铜合金与黄金的是_____(填字母序号)。
A 观察颜色 B 在空气中灼烧 C 滴加稀硫酸 D 滴加硝酸银溶液
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A~F是初中化学常见的物质,其转化关系如图所示(部分反应物和生成物、反应条件已略去)。其中A和D的组成元素相同,且常温下均为无色液体,C为黑色粉末,F是“雪碧”饮料中所含的一种酸 。
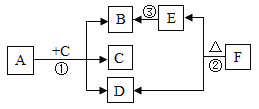
试回答:
(1)反应①的化学表达式为:_________________________, C可能是该反应的______________(填 “反应物”、“生成物” 或 “催化剂”)。
(2)反应②的化学表达式:____________________________,基本类型为________反应。
(3)③是自然界中最重要的反应,称为_____________,它将_________能转变成化学能。
(4)固态的E在生产生活中的用途是________________________________(填一种即可)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】硒元素具有抗衰老、抑制癌细胞生长的功能,其原子结构示意图及在元素周期表中的信息如图,下列说法错误的是( )
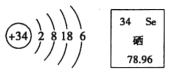
A. 硒原子核内有34个质子
B. 硒元素的相对原子质量是78.96g
C. 硒元素位于元素周期表中第四周期
D. 硒元素在某些化合物中可显-2价
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请根据下列各图中提供的信息回答问题:
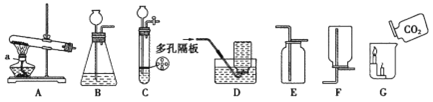
(1)写出仪器a的名称:______。
(2)请写出用装置B制取氧气的化学方程式:______。
(3)比较用过氧化氢溶液和用氯酸钾固体制取O2的方法,两者的共同点是______。
A 发生装置相同
B 都可用MnO2做催化剂
C 完全反应后剩余的固体成分相同
(4)装置B、C都可用来制取二氧化碳,装置C相对于装置B在操作方面的优势是______。
(5)用大理石和稀盐酸制取一瓶二氧化碳气体,将这瓶气体按G所示慢慢倒入烧杯中,观察到蜡烛自下而上依次熄灭,说明二氧化碳具有的性质是______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为了探究二氧化锰是氯酸钾受热分解的催化剂,小红做了如下实验:取两支试管,其中一支加入3克氯酸钾直接加热;另一支加入3克氯酸钾和1克二氧化锰混合后加热。
(1)实验室用加热氯酸钾与二氧化锰混合物的方法制取氧气的文字表达式为___________。
(2)对比未加二氧化锰与加入二氧化锰以后反应速率,其目的是__________;
(3)在实验前后,小红又称量了二氧化锰的质量,其目的是验证在化学反应前后二氧化锰的________是否改变;
(4)反应结束后,小红用反应后的物质中提取得到的二氧化锰再次与氯酸钾混合加热,观察此时二氧化锰能否继续加快反应速率,本实验的目的是探究化学反应前后二氧化锰的________是否改变;
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】“五一”假期,小兵对“锌与硫酸反应快慢的影响因素”进行了探究。
【提出问题】锌与硫酸反应的快慢受哪些因素的影响呢?
【猜想与假设】a.可能与硫酸的质量分数有关;
b.可能与锌的形状有关。
【设计并实验】小兵用不同质量分数的硫酸和不同形状的锌进行如下实验。
实验 编号 | 硫酸的质量 分数(均取 20 mL) | 锌的形状 (均取1 g) | 氢气的体积(mL) (均收集3分钟) |
① | 20% | 锌粒 | 31.7 |
② | 20% | 锌片 | 50.9 |
③ | 30% | 锌粒 | 61.7 |
④ | 30% | 锌片 | 79.9 |
(1)写出稀硫酸与锌反应的化学方程式:________________________。
(2)小兵用如图所示装置收集并测量氢气的体积,其中量筒的作用是________________________________________,氢气应从________(填“e”“f”或“g”)管通入。
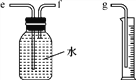
【收集证据】(3)要比较不同质量分数的硫酸对反应快慢的影响,应选择的实验编号是____________。
【得出结论】(4)结论是________________________________________________________________。
(5)下表是小兵第①组实验的详细数据。
时段(均 为1分钟) | 第1 分钟 | 第2 分钟 | 第3 分钟 | 第4 分钟 | 第5 分钟 | 第6 分钟 |
H2的体积 | 3.1 mL | 16.7 mL | 11.9 mL | 9.6 mL | 7.6 mL | 6.0 mL |
请描述锌与硫酸反应的快慢的变化并解释原因:______________________________。
(6)锌与硫酸反应的快慢可能还受哪些因素影响?设计实验验证。___________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】水是生活生产中不可缺少的物质。

①日常生活和生产中常见的水,属于纯净物的是_____。
A 矿泉水 B 蒸馏水 C 河水 D 雨水
②如图甲所示的简易净化水的装置,运用了如下净水方法中的_____(填序号)。
A 消毒 B 过滤 C 蒸馏 D 吸附
③保持水的化学性质的微粒是_____(填名称),图乙中电解水的化学方程式是_____,b 试管中产生的气体是_____,检验该气体的方法是_____,实验说明水是_____由组成的。
④水中滴入几滴石蕊试液,向其中通入二氧化碳气体,可看到石蕊试液变_____色,其反应原理是_____(用化学方程式表示),该原理也可用于制碳酸饮料。打开可乐瓶有大量气泡逸出,说明压强减小,气体溶解度变_____(填“大”或“小”),当气泡逸出后,瓶内的液体_____(填“是”或“不是”)二氧化碳的饱和溶液。
⑤20℃,食盐的溶解度是 36g/100g 水,此时饱和溶液的溶质的质量分数是 26.5%.则“100g”表示_____;“%”表示_____。
A 溶质质量 B 溶剂质量 C 溶液质量 D 溶液体积
⑥将 15g 下列物质投入 85g 水中,使之充分溶解,试比较所得溶液的溶质质量分数的大小_____。
a.二氧化硫 b.氯化钠 c.硫酸铜晶体 d.氧化钙
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化工厂排出的废水中含有硝酸银和硝酸铜。为了测定该废水的组成,取1000g的废水加入锌粉,所得溶液的质量与加入锌粉质量关系如图,请计算:
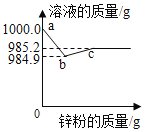
(1)该溶液中硝酸银溶液的质量分数为_____(结果精确到0.1%,下同)。
(2)反应完全后所得溶液的溶质质量分数为_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com