

分析 (1)操作E是过滤操作,结合玻璃棒的作用,进行分析解答.
(2)溶质质量分数变小,则可能是溶质质量偏小或溶剂质量偏大,可以分析出可能造成这两个方面错误的原因进行分析解答.
(3)根据蒸发操作中停止加热的时机,进行分析解答.
(4)根据量筒读数时视线要与凹液面的最低处保持水平进行分析判断.
(5)溶剂的质量分数=1-溶质的质量分数,溶液稀释前后溶质的质量不变,结合题意进行分析解答.
解答 解:(1)操作E是过滤操作,E中玻璃棒的作用是引流.
(2)①氯化钠固体不纯,会造成实际所取的溶质的质量偏小,则使溶质质量分数偏小,故选项正确.
②溶液具有均一性,装瓶时,有少量溶液洒出,溶质质量分数不变,故选项错误.
③量取水时,仰视读数,读数比实际液体体积小,会造成实际量取的水的体积偏大,则使溶质质量分数偏小,故选项正确.
④物码反放,会造成实际所取的溶质的质量偏小,则使溶质质量分数偏小,故选项正确.
(3)蒸发时,待蒸发皿中出现较多量的固体时,应停止加热,利用余热将剩余液体蒸干.
(4)量取液体时,视线与液体的凹液面最低处保持水平,图中俯视刻度,操作错误.
(5)溶剂的质量分数=1-溶质的质量分数,300g16%的氯化钠溶液中溶剂的质量分数为1-16%=84%.
设要加水的质量为x,根据溶液稀释前后溶质的质量不变,
则300g×16%=(300g+x)×10% x=180g.
故答案为:(1)引流;(2)①③④;(3)出现较多量的固体;(4)俯视刻度读数;(5)84%;180g.
点评 本题难度不大,掌握粗盐提纯的步骤与操作注意事项、溶液稀释前后溶质的质量不变等是正确解答本题的关键.


科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
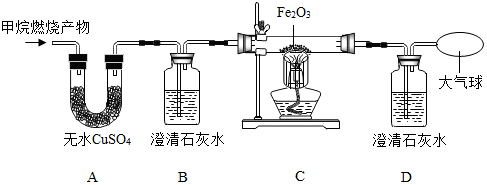
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:推断题
 A、B、C是由碳、氢、氧3种元素组成的单质或化合物,其中A、C组成元素相同,G物质是钙的化合物.它们之间的转化关系如图所示.(“→”表示转化关系,部分反应物、生成物及反应条件已略去)
A、B、C是由碳、氢、氧3种元素组成的单质或化合物,其中A、C组成元素相同,G物质是钙的化合物.它们之间的转化关系如图所示.(“→”表示转化关系,部分反应物、生成物及反应条件已略去)查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 ”表示氢原子,“
”表示氢原子,“ ”表示氧原子,若它们构成的分子在一定条件下发生如下图所示的变化.
”表示氧原子,若它们构成的分子在一定条件下发生如下图所示的变化.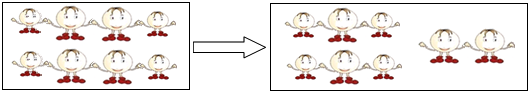
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 主要操作 | 主要现象 | 实验结论 | |
| 甲同学 | 分别将打磨粗细相同的两根R丝插入盛有硫酸铝溶液、硫酸铜溶液AB两只试管中 | B试管中R丝表面覆盖了一层红色的物质,A试管中无现象. | 猜想二成立 |
| 乙同学 | 打磨粗细相同的R丝、铝丝、铜丝,分别将它们插入到体积相同、溶质质量分数也相同的稀硫酸中 | R丝表面产生气泡缓慢,溶液由无色变成蓝色; 铝丝表面产生气泡较快; 铜丝表面没有气泡产生. | 猜想二 成立 写出铝与稀硫酸反应的化学方程式为 2Al+3H2SO4═Al2(SO4)3+3H2↑ |
| 丙同学 | 将铝丝、铜丝分别插入蓝色的RSO4溶液中 | 铝丝、铜丝和溶液都不变色 | 猜想三 成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
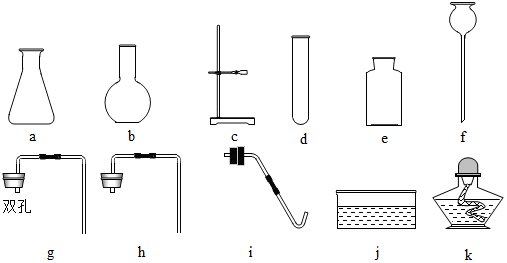

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 某实验小组利用如图所示装置测量空气中氧气体积分数并取得成功.
某实验小组利用如图所示装置测量空气中氧气体积分数并取得成功.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com