
����Ŀ�����ô����������������ԭ���ȵ�����ͭ���ⶨˮ����ɡ�ʵ��װ����A��B��C��D��ɣ���������װ��ʡ��δ���������ش��������⣺
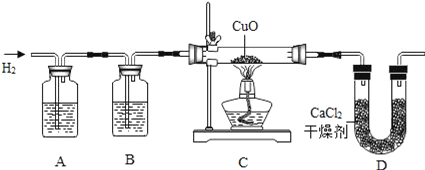
��1�����ijѧ����п�ͽ�Ũ��������ȡ����������װ��A��B��Ϊ�˵õ��������������������װ��A��ͨ����_____��Һ����������_____����װ��B��ͨ����_____��Һ����������_____��
��2����ʵ��ǰ����������£�װ����ͭ�IJ����ܵ���������6.4�ˣ�װ�Ȼ��Ƶ�U�ܵ�����������7.2�ˡ���������ʵ�����ݣ�д��ˮ���⡢������Ԫ�ص�����_____��
��3����װ��D�У���CaCl2�Ļ�Ϊ��ˮ����ͭ������Ϊ_____��
���𰸡�NaOH����AgNO3�� ����HCl���� Ũ���� �������� ��7.2g��6.4g����6.4g ��ɫ����ˮ����ͭ����ɫ
��������
��1������������ԭ����ͭ����ˮ��ͭ������ͼʾ��������������п�ͽ�Ũ�����ᷴӦ�Ƶã��������к����Ȼ��������ˮ��������Ҫ��ȥ���ǣ���װ��A��ͨ��������������Һ���������������Ȼ������巴Ӧ�����Ȼ�����Һ���������������Ȼ������壻��װ��B��ͨ����Ũ������Һ��������ˮ�ԣ�������������������ǣ�����������
��2��U�ιܼ����������C���Թܼ���������������ɵ�ˮ����Ԫ�ص�������D���ؼ����ɵ�ˮ��������ˮ���⡢������Ԫ�ص�������7.2g��6.4g����6.4g =1:8��
��3��ˮ��ʹ��ɫ����ˮ����ͭ����ɫ����������ˮ����ͭ����ˮ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼ������ȷ��ӳ��Ӧ�仯��ϵ�ĸ�����( )
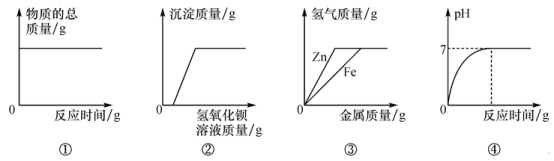
�ٺ������ܱ�������ȼ��
������������ƵĻ����Һ����μ�������������Һ
�۵�������������������ϡ�����зֱ�������п�ۺ�����
��һ��������ϡ�����У���μ�����ϡ���������������������������������Һ
A.1��B.2��C.3��D.4��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼΪ�����ȵ�ʾ��ͼ��
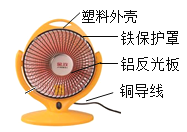
(1)�������к��еĽ�����_____(�ѧʽ��дһ�ּ���)��
(2)�������ֳ���ʹ������ʴ��ԭ����_____��
(3)�������ֳ�����ˢ��ķ������⣬�����ԭ����_____��
(4)��д��һ������������ͭ�Ľ������ǿ���Ļ�ѧ����ʽ_____��
(5)ȡů�����Ϻ�����Ϊ����Ĵ���������_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ԫ�ػ��ϼ۷����ı�ķ�Ӧ����������ԭ��Ӧ�����з�Ӧ������������ԭ��Ӧ����
A.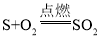
B.![]()
C.![]()
D.
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������Ͻ�����Ҫ�Ĺ�ҵ���������ϡ��±���A��B��C���ֽ����IJ����������ʡ�
���� ���� | �����ԣ�100Ϊ���� | �ܶȣ�g/cm3 �� | �۵㣨�棩 | Ӳ�ȣ�10Ϊ���� |
A | 99 | 8.92 | 1083 | 3 |
B | 61 | 2.70 | 660 | 2.9 |
C | 17 | 7.86 | 1535 | 5 |
��1�����ֽ���������������ߵ���____________������ĸ��ţ�����ѹ����߲��ý���A��ѡ�ý���B����Ҫԭ����__________________��
��2��C�ĺϽ�ͨ���������˵������ӵȣ���Ͻ��Ӳ��_______________5����������������������������
��3���ѣ�Ti�����ѺϽ���Ϊ��21������Ҫ�Ľ������ϡ��Խ��ʯ����Ҫ������TiO2��Ϊԭ�������ѵIJ����У����ڸ����£�����ʯ�뽹̿�Ļ������ͨ��������Cl2�����õ�TiCl4��һ�ֿ�ȼ�����塣����ϡ�����廷���ͼ��������£���Mg��TiCl4��Ӧ�õ�Ti��MgCl2�����в������еĻ�ѧ����ʽΪ_��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ŀǰ���ĵ���Դ��Ҫ���Ի�ʯȼ�ϡ�
��1��ʯ���ǻ�ʯȼ��֮һ��������_______��������������������������������Դ��
��2��ú�龭���鴦�����ڿ�����ȼ�յø��졢����֣�������Ϊ________��
��3�����е�ȼ�����칤�̣�ʹ����ľ�����������Ȼ������Ȼ��ȼ�յĻ�ѧ����ʽΪ_____�����÷��ˣ��ر�ȼ������ʹ����Ϩ���ԭ����_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ķ��������ϣ��ش�������⣺
Ŀǰ�������ϵ��ƶ������õ�������Ȼ��Ƶķ����Ƶá��Ȼ��Ƶ��۵�Ϊ801�棬�ڼ����������ѡ����Ȼ��ƺ��Ȼ��ư�������2��3��Ϲ��ۣ��ɵõ������¶�ԼΪ580��Ĺ���������˵��������¶ȡ����ʱ�������������ų��������ƺͽ�����ͬʱ����ԭ���������ڸ����Ĺ������ϣ��ӹܵ�����������ڵĽ����������ȴ��105��110�棬�����Ƴɾ��������������˷��롣
��ԭ�ӵĽṹʾ��ͼΪ![]() �����Խ����ƵĻ�ѧ���ʺܻ��ã��ڿ����м��ױ������������ƣ���С��һ�У���¶�����ı�����Ŀ������ɫ�н��������ƻ�����ˮ��Ӧ�������������ƺ�������ʵ�����еĽ�����ͨ��������ʯ�����С�
�����Խ����ƵĻ�ѧ���ʺܻ��ã��ڿ����м��ױ������������ƣ���С��һ�У���¶�����ı�����Ŀ������ɫ�н��������ƻ�����ˮ��Ӧ�������������ƺ�������ʵ�����еĽ�����ͨ��������ʯ�����С�
�����Ƶ�Ӧ�÷dz��㷺���ֽ�������������һ�ֿ������������һ�Ǧ�����ܽ������͵ı����ԡ��ƻ���������������ƣ�Na2O2���Ȼ�����ƺͼ���ɵĺϽ��ڳ���ʱ��Һ�壬���ڿ�������ֳ��Ӧ�����Ƚ������塣
��1�����Ƶ�ԭ�ӽṹ�У����仯ѧ���ʻ��ù�ϵ�����е�������_________________��
��2��������ͨ��������ʯ�����У�Ŀ���Ǹ���_____________________��
��3��������ˮ��Ӧ����ѧ����ʽΪ__________________________________________���Ʋ���ܲ�����ˮ��Ӧ��˵������__________________________________________��
��4�����������ܽ��ƾ��е�����������__________________________________________��д��4������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ܶ����϶����������ᣨC6H8O7�������й����������˵������ȷ���ǣ� ��
A.����������
B.��������̼���⡢������Ԫ�ص�������Ϊ9:1:14
C.19.2g��������̼Ԫ�ص�������1.2g
D.��������������Ԫ�ص���������Ϊ![]() ��100%
��100%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͼ1ΪNaCl��KNO3���ܽ�����ߡ�
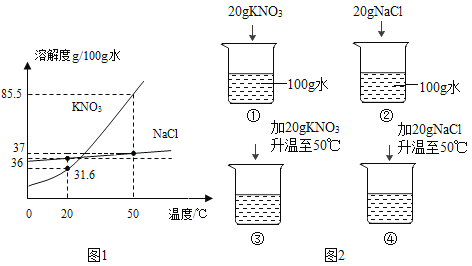
��1��20��ʱ��KNO3���ܽ����_______��
��2��50��ʱ����50gKNO3������뵽50gˮ�еõ�����KNO3��_______������͡������͡�����Һ����ʱ��Һ����������������_______��������0.1%��
��3����ȥNaCl��Һ�л���������KNO3���ᴿNaCl�ķ�����_______��
��4��20��ʱ��ijͬѧ������ͼ2ʵ�飬�õ���Ӧ��Һ��~�ܣ�˵����ȷ����______��
A�٢�����Һ�����������������
B�ۢ�����Һ�����������������
C���ۢܽ�����20�棬���о���������m(KNO3)��m(NaCl)
D���ۢܽ�����20�棬���ʵ������ۣ���
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com