
“五一”假期,小兵对“锌与硫酸反应快慢的影响因素”进行了探究。
【提出问题】锌与硫酸反应的快慢受哪些因素的影响呢?
【猜想与假设】a.可能与硫酸的质量分数有关;b.可能与锌的形状有关。
【设计并实验】小兵用不同质量分数的硫酸和不同形状的锌进行如下实验。
|
实验编号 |
硫酸的质量分数(均取20mL) |
锌的形状(均取1g) |
氢气的体积(mL)(均收集3分钟) |
|
|
20% |
锌粒 |
31.7 |
|
|
20% |
锌片 |
50.9 |
|
|
30% |
锌粒 |
61.7 |
|
|
30% |
锌片 |
79.9 |
(1)写出稀硫酸与锌反应的化学方程式 。
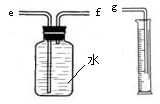
(2)小兵用下图装置收集并测量氢气的体积,其中量筒的作用是 。

【收集证据】(3)要比较不同质量分数的硫酸对反应快慢的影响,应选择的实验编号是 。
【得出结论】(4)结论是 。
【评价与反思】
(5)下表是小兵第①组实验的详细数据。
|
时段(均为1分钟) |
第1分钟 |
第2分钟 |
第3分钟 |
第4分钟 |
第5分钟 |
第6分钟 |
|
H2的体积 |
3.1mL |
16.7mL |
11.9mL |
9.6mL |
7.6mL |
6.0mL |
请描述锌与硫酸反应的快慢的变化并解释原因 。
(6)锌与硫酸反应的快慢可能还受哪些因素影响? 。
(1)Zn + H2SO4 = ZnSO4 + H2↑
(2)通过测量排出水的体积,即产生氢气体积
(3)①③或②④
(4)硫酸的质量分数越大反应越快,锌片比锌粒反应快
(5)第1分钟反应慢,因为锌粒表面有氧化膜、油污等,覆盖在锌粒表面,从第2分钟以后,随着反应的进行,硫酸的质量分数减少,反应逐渐变慢
(6)温度或催化剂等
【解析】
试题分析:(1)稀硫酸与锌反应的化学方程式:Zn + H2SO4 = ZnSO4 + H2↑
(2)装置的连接顺序是f→e→g,通过氢气将水排到量筒内,所以量筒的作用是通过测量排出水的体积,即产生氢气体积
(3)要比较不同质量分数的硫酸对反应快慢的影响,那就要控制其他的量要相同,所以选择①③或②④
(4)通过①③或②④比较,随着硫酸质量分数的增大,在3分钟内收集到的氢气体积也增多了,所以可以得出结论:硫酸的质量分数越大反应越快,通过①②或③④比较,可得出结论:锌片比锌粒反应快
(5)第1分钟反应慢,因为锌粒表面有氧化膜、油污等,覆盖在锌粒表面,从第2分钟以后,随着反应的进行,硫酸的质量分数减少,反应逐渐变慢
(6)影响锌与硫酸反应的快慢的因素很多;比如温度或催化剂等
考点:金属与酸反应速率快慢的影响因素的探究


科目:初中化学 来源: 题型:阅读理解
| 实验编号 | 硫酸的质量分数(均取20mL) | 锌的形状(均取1g) | 氢气的体积(mL)(均收集3分钟) |
| ① | 20% | 锌粒 | 31.7 |
| ② | 20% | 锌片 | 50.9 |
| ③ | 30% | 锌粒 | 61.7 |
| ④ | 30% | 锌片 | 79.9 |

| 时段(均为1分钟) | 第1分钟 | 第2分钟 | 第3分钟 | 第4分钟 | 第5分钟 | 第6分钟 |
| H2的体积 | 3.1mL | 16.7mL | 11.9mL | 9.6mL | 7.6mL | 6.0mL |
查看答案和解析>>
科目:初中化学 来源:2013年初中毕业升学考试(安徽卷)化学(带解析) 题型:问答题
“五一”假期,小兵对“锌与硫酸反应快慢的影响因素”进行了探究。
【提出问题】锌与硫酸反应的快慢受哪些因素的影响呢?
【猜想与假设】a.可能与硫酸的质量分数有关;b.可能与锌的形状有关。
【设计并实验】小兵用不同质量分数的硫酸和不同形状的锌进行如下实验。
| 实验编号 | 硫酸的质量分数(均取20mL) | 锌的形状(均取1g) | 氢气的体积(mL)(均收集3分钟) |
| ① | 20% | 锌粒 | 31.7 |
| ② | 20% | 锌片 | 50.9 |
| ③ | 20% | 锌粒 | 61.7 |
| ④ | 30% | 锌片 | 79.9 |
| 时段(均为1分钟) | 第1分钟 | 第2分钟 | 第3分钟 | 第4分钟 | 第5分钟 | 第6分钟 |
| H2的体积 | 3.1mL | 16.7mL | 11.9mL | 9.6mL | 7.6mL | 6.0mL |
查看答案和解析>>
科目:初中化学 来源: 题型:
“五一”假期,小兵对“锌与硫酸反应快慢的影响因素”进行了探究。
【提出问题】锌与硫酸反应的快慢受哪些因素的影响呢?
【猜想与假设】a.可能与硫酸的质量分数有关;b.可能与锌的形状有关。
【设计并实验】小兵用不同质量分数的硫酸和不同形状的锌进行如下实验。
| 实验编号 | 硫酸的质量分数(均取20mL) | 锌的形状(均取1g) | 氢气的体积(mL)(均收集3分钟) |
| ① | 20% | 锌粒 | 31.7 |
| ② | 20% | 锌片 | 50.9 |
| ③ | 20% | 锌粒 | 61.7 |
| ④ | 30% | 锌片 | 79.9 |
(1)写出稀硫酸与锌反应的化学方程式___________________________________________。
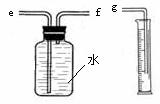 (2)小兵用右图装置收集并测量氢气的体积,其中量筒的作用是_______________________,氢气应从________(填e或f或g)管通入。
(2)小兵用右图装置收集并测量氢气的体积,其中量筒的作用是_______________________,氢气应从________(填e或f或g)管通入。
【收集证据】(3)要比较不同质量分数的硫酸对反应快慢的影响,应选择的实验编号是____________。
【得出结论】(4)结论是________________________________
____________________________________________________________________________。
【评价与反思】(注意:若答对(5)(6)两小题奖励4分,化学试卷总分不超过60分)
(5)下表是小兵第①组实验的详细数据。
| 时段(均为1分钟) | 第1分钟 | 第2分钟 | 第3分钟 | 第4分钟 | 第5分钟 | 第6分钟 |
| H2的体积 | 3.1mL | 16.7mL | 11.9mL | 9.6mL | 7.6mL | 6.0mL |
请描述锌与硫酸反应的快慢的变化并解释原因______________________________________
_____________________________________________________________________________。
(6)锌与硫酸反应的快慢可能还受哪些因素影响?设计实验验证。___________________
___________________________________________________________________________________________________________________________________________________________。
查看答案和解析>>
科目:初中化学 来源:2013年安徽省中考化学试卷(解析版) 题型:解答题
| 实验编号 | 硫酸的质量分数(均取20mL) | 锌的形状(均取1g) | 氢气的体积(mL)(均收集3分钟) |
| ① | 20% | 锌粒 | 31.7 |
| ② | 20% | 锌片 | 50.9 |
| ③ | 30% | 锌粒 | 61.7 |
| ④ | 30% | 锌片 | 79.9 |
| 时段(均为1分钟) | 第1分钟 | 第2分钟 | 第3分钟 | 第4分钟 | 第5分钟 | 第6分钟 |
| H2的体积 | 3.1mL | 16.7mL | 11.9mL | 9.6mL | 7.6mL | 6.0mL |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com