
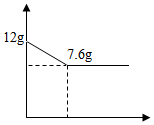
 将12g石灰石放入足量的稀盐酸中,(杂质不反应)完全反应后,如图所示:
将12g石灰石放入足量的稀盐酸中,(杂质不反应)完全反应后,如图所示:分析 (1)利用质量守恒定律,可由反应前后质量差求出放出二氧化碳的质量;
(2)根据反应的化学方程式,计算参加反应碳酸钙质量,从而求得石灰石中CaCO3的质量分数.
解答 解:(1)生成二氧化碳的质量为:12g-7.6g=4.4g;故填:4.4g;
(2)设参加反应的碳酸钙的质量为x.
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 4.4g
$\frac{100}{x}=\frac{44}{4.4g}$
x=10g
石灰石中CaCO3的质量分数=$\frac{10g}{12g}$×100%=83.3%
答::石灰石中CaCO3的质量分数为83.3%.
点评 根据质量守恒定律分析得反应放出二氧化碳的质量,此为解答本题的计算基础,体现出对问题的分析能力.


科目:初中化学 来源: 题型:选择题
| A. | 食盐溶液和稀盐酸 | B. | 氢氧化钾溶液和硫酸溶液 | ||
| C. | 碳酸钠溶液和稀盐酸 | D. | 石灰水和碳酸钾溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
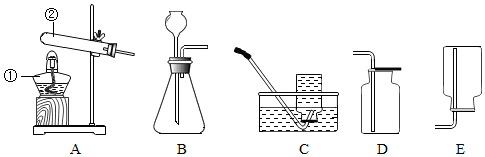
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
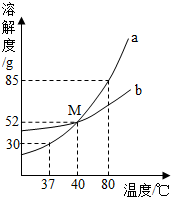 如图为a、b两种物质的溶解度曲线.请根据图中内容回答下列问题:
如图为a、b两种物质的溶解度曲线.请根据图中内容回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 如图,小新同学将学校荷花池中浑浊的水样倒入烧杯中,先加入明矾粉末搅拌溶解,静置一会儿,采用如图的装置进行过滤.加明矾的作用是加速沉降.图中缺少的一种仪器是玻璃棒,其作用是引流;
如图,小新同学将学校荷花池中浑浊的水样倒入烧杯中,先加入明矾粉末搅拌溶解,静置一会儿,采用如图的装置进行过滤.加明矾的作用是加速沉降.图中缺少的一种仪器是玻璃棒,其作用是引流;查看答案和解析>>
科目:初中化学 来源: 题型:推断题
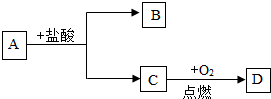 已知A、B、C、D四种物质之间存在以下转化关系,其中AC是单质,B为浅绿色溶液,D是相对分子质量最小的氧化物,试回答:
已知A、B、C、D四种物质之间存在以下转化关系,其中AC是单质,B为浅绿色溶液,D是相对分子质量最小的氧化物,试回答:查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com