
| A. | 酸能使紫色石蕊试液变红,紫色石蕊试液中通入CO2后变红,故CO2是酸 | |
| B. | 酸性溶液的pH小于7,食醋呈酸性,故食醋的pH小于7 | |
| C. | 在同一化合物中,金属元素显正价,故非金属元素一定显负价 | |
| D. | 改变条件,使溶液中有晶体析出,溶质质量减少,故溶液的质量分数一定减小 |
分析 二氧化碳本身不显酸性,与水反应生成的碳酸呈酸性,酸性溶液的pH小于7,非金属元素既有正价也有负价,析出晶体的方法不确定,则溶质质量分数的变化也不确定.
解答 解:
A、二氧化碳与水反应生成的碳酸显酸性,能使石蕊变红,并不能说明二氧化碳是酸,故错误;
B、酸性溶液的pH小于7.食醋是酸性溶液,所以食醋的pH小于7,推理正确,故正确;
C、在同一化合物中,金属元素显正价,非金属元素既有正价又有负价,故C错误;
D、饱和溶液中析出晶体,若是温度不变蒸发溶剂,则溶液仍处于饱和状态,溶质和溶液的比值不变,则溶质的质量分数不变,故D错误.
故选B.
点评 此题是对多个知识点的考查,主要是能对相关的知识有较全面的了解,加强概念的识记及理解,以便灵活应用.


 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:初中化学 来源: 题型:解答题
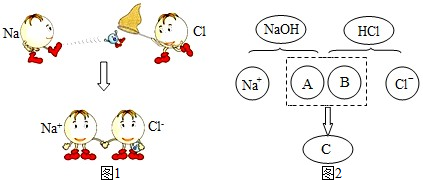
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | CO(NH2)2、KNO3都属于氮肥 | B. | 氢能、风能、太阳能都属于清洁能源 | ||
| C. | 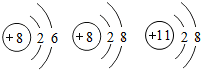 都表示阳离子 都表示阳离子 | D. | 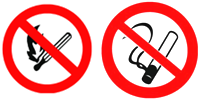 都不是公共场所禁止吸烟的图标 都不是公共场所禁止吸烟的图标 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 序号 | 目标 | 方法 |
| A | 二氧化碳中混有少量一氧化碳 | 点燃 |
| B | 一氧化碳中混有少量二氧化碳 | 通过澄清石灰水 |
| C | 铜粉中混有少量铁粉 | 加入足量稀盐酸再过滤 |
| D | 氯化亚铁溶液中混有少量氯化铜 | 加入足量铁粉并过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 实验室用溶质质量分数为10%硫酸钠溶液进行水的电解实验.
实验室用溶质质量分数为10%硫酸钠溶液进行水的电解实验.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
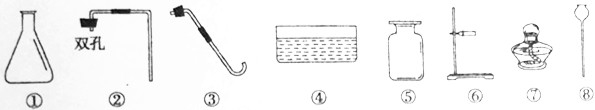
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

| 装置编号 | 实验现象 |
| ① | 金属表面无明显现象 |
| ② | 剧烈反应,金属表面产生大量无色气泡,每片逐渐溶解 |
| ③ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
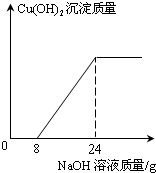 化学兴趣小组的同学监测到一工厂排放的废水中含有H2SO4和CuSO4.为了测定废水中CuSO4的质量分数,该小组取了200g废水,逐滴加入20%的NaOH溶液至过量.测得生成Cu(OH)2沉淀的质量与所加NaOH溶液质量的关系如图所示.
化学兴趣小组的同学监测到一工厂排放的废水中含有H2SO4和CuSO4.为了测定废水中CuSO4的质量分数,该小组取了200g废水,逐滴加入20%的NaOH溶液至过量.测得生成Cu(OH)2沉淀的质量与所加NaOH溶液质量的关系如图所示.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
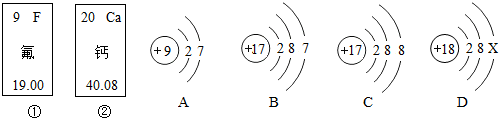
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com