
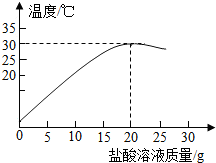
 (2013?如皋市模拟)某化学兴趣小组的同学在实验室配制溶质质量分数为7.3%的稀盐酸,并用其测定某氢氧化钠溶液溶质的质量分数.右图表示用上述配制的稀盐酸与20g某氢氧化钠溶液发生反应过程中,使用数字传感仪测得溶液温度变化的曲线.
(2013?如皋市模拟)某化学兴趣小组的同学在实验室配制溶质质量分数为7.3%的稀盐酸,并用其测定某氢氧化钠溶液溶质的质量分数.右图表示用上述配制的稀盐酸与20g某氢氧化钠溶液发生反应过程中,使用数字传感仪测得溶液温度变化的曲线.| 40 |
| 36.5 |
| X |
| 1.46g |
| 1.6g |
| 20g |


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:

| ||
| ||
| 催化剂 |
| 氧气 |
| 水 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
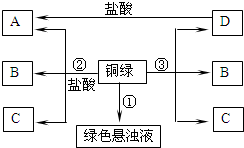 (2013?如皋市模拟)小彤的一副眼镜戴了一段时间后,发现铜质镜架上出现了一层绿色物质,他想将其除掉.经查阅资料得知:铜在一定条件下会锈蚀生成一种绿色物质,其主要成分是碱式碳酸铜[俗称铜绿,化学式为Cu2(OH)2CO3],该物质受热不稳定易分解.他根据元素守恒分析,得出铜生锈是铜与空气中的氧气、二氧化碳和
(2013?如皋市模拟)小彤的一副眼镜戴了一段时间后,发现铜质镜架上出现了一层绿色物质,他想将其除掉.经查阅资料得知:铜在一定条件下会锈蚀生成一种绿色物质,其主要成分是碱式碳酸铜[俗称铜绿,化学式为Cu2(OH)2CO3],该物质受热不稳定易分解.他根据元素守恒分析,得出铜生锈是铜与空气中的氧气、二氧化碳和
| ||
| ||
| ||
| ||
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com