
| A. | 盐:小苏打、硫酸铜、硝酸铵 | B. | 无机物:H2O、CaCO3、C2H3OH | ||
| C. | 混合物:冰水共存物、石油、熟石灰 | D. | 合成材料:塑料、合成纤维、合金 |
分析 A.根据盐的概念来分析;
B.根据无机物的概念来分析;
C.根据混合物的概念来分析;
D.根据合成材料的分类来分析.
解答 解:A.小苏打是由钠离子和碳酸氢根离子构成的化合物,硫酸铜是由铜离子和硫酸根离子构成的化合物,硝酸铵是由铵根离子和硝酸根离子构成的化合物,均属于盐,故正确;
B.H2O中不含碳元素,属于无机物,CaCO3虽然含有碳元素,但仍然属于无机物,C2H3OH是一种含碳元素的化合物,属于有机物,故错误;
C.冰水混合物中只含水这一种物质,属于纯净物,故错误;
D.合成材料包括塑料、合成纤维和合成橡胶,合金属于金属材料,故错误.
故选A.
点评 解答本题关键是要知道混合物、盐、合成材料的概念,熟悉无机物与有机物的判断方法.


科目:初中化学 来源: 题型:推断题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
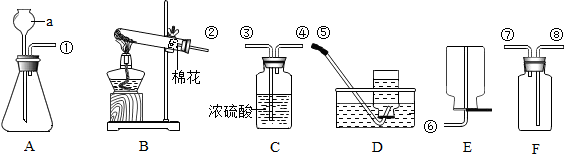
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
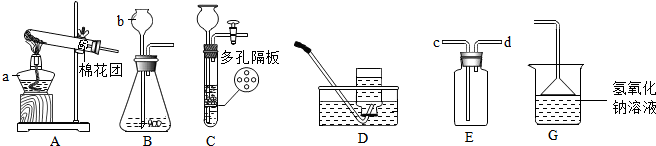
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 该物质是一种遇热不稳定的有机化合物 | |
| B. | 该物质受热后易发生化学变化 | |
| C. | 该物质的相对分子质量为100 | |
| D. | 该物质含氟的质量分数为76% |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 物质 | 所含杂质 | 除去杂质的方法 |
| A | CO2 | HCl | 依次通过足量的NaOH溶液和浓硫酸 |
| B | FeSO4溶液 | CuSO4 | 加入足量的锌粒,充分反应,过滤 |
| C | NaCl溶液 | Na2CO3 | 加入适量的澄清石灰水,过滤 |
| D | KCl | MnO2 | 加水充分溶解,过滤,蒸发结晶 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

| 实验步骤 | 观察到的现象 | 获得结论 | 有关反应的化学方程式 |
| 取少量黑色粉末于试管中,向其中加入足量的稀硫酸,振荡 | 固体完全溶解,溶液变蓝 | 黑色粉末均为氧化铜 | CuO+H2SO4=CuSO4+H2O |

| 反应前 | 反应后 |
| 玻璃管和内盛氧化铜粉末的总质量为62.0g | 玻璃管和内盛红色粉末的总质量为61.7g |
| 玻璃管的质量为60.0g | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com