
| 10g-3.5g |
| 10g |
| 65 |
| 6.5g |
| 2 |
| x |


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:
| 序号 | 加入稀盐酸的质量/g | 剩余固体的质量/g |
| 第1次 | 25 | 11 |
| 第2次 | 25 | 6 |
| 第3次 | 25 | n |
| 第4次 | 25 | 2.8 |
查看答案和解析>>
科目:初中化学 来源: 题型:
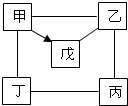 如图中“--”表示相连的物质间在一定条件下可以反应,“→”表示甲在一定条件下可以转化为戊,甲、乙、丙、丁、戊分别为Mg、MgO、H2SO4、NaOH、CuCl2五种物质中的一种,回答下列问题:
如图中“--”表示相连的物质间在一定条件下可以反应,“→”表示甲在一定条件下可以转化为戊,甲、乙、丙、丁、戊分别为Mg、MgO、H2SO4、NaOH、CuCl2五种物质中的一种,回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
 如图为某种补锌口服液说明书的一部分,请回答:
如图为某种补锌口服液说明书的一部分,请回答:查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com