
分析 (1)根据常见的化学仪器的名称,进行分析解答.
(2)氯酸钾在二氧化锰的催化作用下生成氯化钾和氧气,写出反应的化学方程式即可.
(3)根据实验室中制取二氧化碳的反应原理和反应条件来选择反应的发生装置,根据二氧化碳的密度及水溶性来选择收集装置,结合二氧化碳的验满方法、分液漏斗能控制滴加液体的速率,进行分析解答.
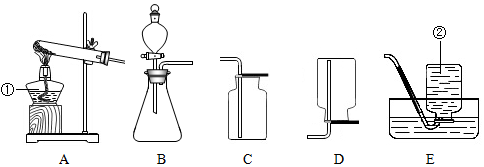
解答 解:(1)仪器①是酒精灯;仪器②是集气瓶.
(2)氯酸钾在二氧化锰的催化作用下生成氯化钾和氧气,反应的化学方程式为:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.
(3)实验室中制取二氧化碳常用大理石或石灰石和稀盐酸反应来制取,属于固液常温型,所以应该选择B装置来制取二氧化碳气体;二氧化碳密度比空气大,能溶于水,应用向上排空气法收集,所以应该选择C装置来收集二氧化碳.
验满二氧化碳的方法是将燃着的木条放在集气瓶口,若木条熄灭,说明已集满二氧化碳.
装置B中用分液漏斗代替长颈漏斗的优点是能通过控制滴加液体的速率,控制反应的速率.
故答案为:(1)酒精灯;集气瓶;
(2)2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;
(3)B和C;将燃着的木条放在集气瓶口,若木条熄灭,说明已集满二氧化碳;能通过控制滴加液体的速率,控制反应的速率.
点评 本题难度不大,是中考的重要考点之一,熟练掌握实验室中制取气体的反应原理、发生装置和收集装置的选择依据等是正确解答本题的关键.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 物质 | 操作方法 |
| A | Fe(Cu) | 加入过量稀盐酸,充分反应后过滤 |
| B | CaO 粉末(CaCO3 粉末) | 高温煅烧 |
| C | NaOH 溶液(Ca(OH)2 溶液) | 通入 CO2 气体,充分反应后过滤 |
| D | NaCl 溶液(CuSO4 溶液) | 通入过量 Ba(OH)2 溶液,充分反应后过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
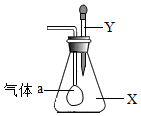 如图所示,锥形瓶内盛有气体X,滴管内盛有液体Y,若挤压滴管胶头,使液体Y滴入瓶中,振荡,一会儿可见小气球a鼓起.气体X和液体Y可能是( )
如图所示,锥形瓶内盛有气体X,滴管内盛有液体Y,若挤压滴管胶头,使液体Y滴入瓶中,振荡,一会儿可见小气球a鼓起.气体X和液体Y可能是( )| A. | X是CO2,Y是氢氧化钠 | B. | X是O2,Y是稀H2SO4(稀硫酸) | ||
| C. | X是N2,Y是稀盐酸 | D. | X是CO,Y是氢氧化钠 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| OH- | NO3- | Cl- | SO42- | |
| H+ | 溶、挥 | 溶、挥 | 溶 | |
| K+ | 溶 | 溶 | 溶 | 溶 |
| Mg2+ | 不溶 | 溶 | 溶 | 溶 |
| Mn2+ | 不溶 | 溶 | 溶 | 溶 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
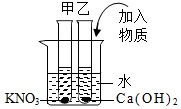 表为硝酸钾和氢氧化钙在不同温度下的溶解度.如图所示,甲、乙试管分别盛有20℃时硝酸钾、氢氧化钙的饱和溶液,试管底部均有未溶解的固体.现向烧杯内的水中加入某物质后,甲试管中固体消失,乙试管中固体增加,则加入的物质可能是( )
表为硝酸钾和氢氧化钙在不同温度下的溶解度.如图所示,甲、乙试管分别盛有20℃时硝酸钾、氢氧化钙的饱和溶液,试管底部均有未溶解的固体.现向烧杯内的水中加入某物质后,甲试管中固体消失,乙试管中固体增加,则加入的物质可能是( )| 温度(℃) | 10 | 20 | 40 | 60 | 80 |
| 氢氧化钙的质量(温度) | 0.173 | 0.165 | 0.121 | 0.120 | 0.095 |
| 硝酸钾的质量 | 13.3 | 31.6 | 63.9 | 110 | 169 |
| A. | 硝酸铵 | B. | 氢氧化钠 | C. | 蔗糖 | D. | 氯化钠 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 滤出的固体中一定含有银,一定不含铁 | |
| B. | 滤出的固体中一定含有银,可能含有铜 | |
| C. | 滤液中一定有硝酸银,可能有硝酸铜 | |
| D. | 滤液中若有硝酸银,则一定有硝酸铜 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com