
| 盐酸质量/g | 36.5 | 73 | 109.5 | 146 |
| 气体质量/g | 0.1 | 0.2 | 0.2 | m |

 ×100%即可求出生铁中铁的质量分数.
×100%即可求出生铁中铁的质量分数.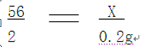


科目:初中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:初中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:初中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:初中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:初中化学 来源:不详 题型:计算题
 Zn+2Cu+2CO2↑)然后加工成“黄金”饰品出售,非法牟取利益。作为当代中学生,请你利用所学知识揭露“伪黄金”的庐山真面目。
Zn+2Cu+2CO2↑)然后加工成“黄金”饰品出售,非法牟取利益。作为当代中学生,请你利用所学知识揭露“伪黄金”的庐山真面目。查看答案和解析>>
科目:初中化学 来源:不详 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com