
| A. | 细铁丝在氧气中燃烧时集气瓶底炸裂--集气瓶底部未放入少量水或细沙 | |
| B. | 加热碱式碳酸铜粉末时试管破裂--试管口未向上倾斜 | |
| C. | 用pH试纸测定稀盐酸的pH值偏大一pH试纸预先用水润湿 | |
| D. | 加热高锰酸钾制氧气时水倒吸入试管--先熄灭酒精灯后撤导管 |
分析 A、根据细铁丝在氧气中燃烧实验时熔化的溅落物会炸裂瓶底进行分析判断.
B、根据给试管里的固体加热时,试管口未向下倾斜可能会使试管炸裂解答;
C、根据pH试纸的使用及酸性的强弱与pH的关系分析;
D、根据制取氧气的注意事项分析.
解答 解:A、细铁丝在氧气中燃烧时,为了防止高温生成物直接落在瓶底而使瓶底炸裂,需要在集气瓶底放少量水或铺一层细沙;故分析合理.
B、给试管里的固体加热时,试管口未向下倾斜可能会使试管炸裂,而不是向上倾斜,故分析不合理;
C、pH试纸预先用水润湿,会使盐酸的酸性减弱,pH偏大,故分析合理;
D、加热高锰酸钾制氧气时先熄灭酒精灯后撤导管,会引起水的倒流,故分析合理;
故选项为:B.
点评 本题难度不大,掌握常见化学实验操作的注意事项、实验数据处理或者误差分析的探究方法是正确解答本题的关键.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:实验探究题
 A、B、C、D和甲、乙均为初中化学中常见的物质,物质间存在着如图所示的相互转化关系(部分生成物未标出).请回答下列问题:
A、B、C、D和甲、乙均为初中化学中常见的物质,物质间存在着如图所示的相互转化关系(部分生成物未标出).请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 混合物、氧化物、盐 | B. | 混合物、盐、化合物 | ||
| C. | 单质、混合物、盐 | D. | 金属单质、氧化物、纯净物 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验步骤 | 实验现象 | 解释或结论 |
| ①取适量烧碱样品置于试管中,加水溶解,并用手触摸试管外壁 | 试管外壁发热 | 原因是:氢氧化钠固体.溶于水放热 |
| ②向①所得的溶液中逐滴加入稀硝酸至过量 | 开始无明显现象,一段时间后产生能使澄清石灰水变浑浊的气体 | 样品中含有的杂质是Na2CO3. |
| ③向②所得的溶液中滴加几滴硝酸银溶液 | 产生白色沉淀现象 | 样品中还含有的杂质是NaCl. |
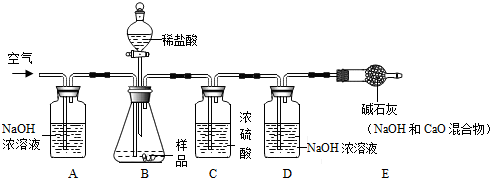
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 向盛有100g不饱和Na2CO3溶液的烧杯中,滴入一定量的BaCl2溶液至恰好完全反应,然后过滤,将得到的固体物质放入烧杯中,并向其中逐滴滴入溶质质量分数为10%的稀盐酸,烧杯中难溶物质的质量与所滴入稀盐酸的质量关系曲线如图所示.请根据题意回答下列问题:
向盛有100g不饱和Na2CO3溶液的烧杯中,滴入一定量的BaCl2溶液至恰好完全反应,然后过滤,将得到的固体物质放入烧杯中,并向其中逐滴滴入溶质质量分数为10%的稀盐酸,烧杯中难溶物质的质量与所滴入稀盐酸的质量关系曲线如图所示.请根据题意回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 蒸发滤液时,待蒸发皿中滤液蒸干后停止加热 | |
| B. | 粗盐溶解和过滤操作时,都用到了玻璃棒,玻璃棒的作用相同 | |
| C. | 配制该溶液需要氯化钠8g,水42g | |
| D. | 配制溶液需要经过计算、称量、量取、溶解、装瓶、贴标签等步骤 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
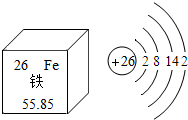 化学是一门研究物质的科学,我们一般从物质的存在、性质、制备、用途等方面研究一种物质或一类物质.以金属铁为例.请你参与其中回答相关问题:
化学是一门研究物质的科学,我们一般从物质的存在、性质、制备、用途等方面研究一种物质或一类物质.以金属铁为例.请你参与其中回答相关问题: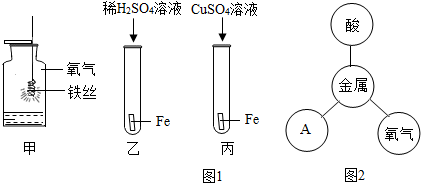
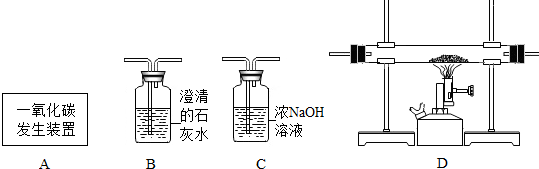
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com