
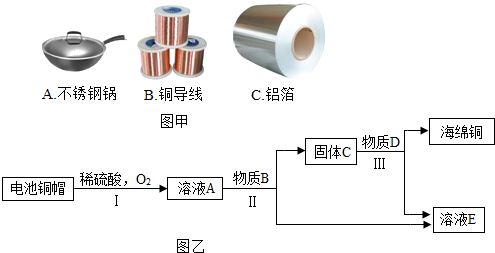
分析 (1)根据金属具有导电性,可以用作导线,具有导热性,可以用于制成炊具,铝具有延展性,可以制成铝箔进行分析;
(2)根据元素化合价的变化判断氧化剂和还原剂,硫酸铜和铁反应生成硫酸亚铁和铜,以及氢氧化铝中铝元素的质量分数进行分析;
(3)根据过滤可以把不溶于水的物质除去进行分析;
铜和氧气、稀硫酸反应生成硫酸铜和水,锌和稀硫酸反应生成硫酸锌和氢气,溶液A中含有硫酸铜和硫酸锌;
向溶液A中加入过量的锌时,锌能和硫酸铜反应生成硫酸锌和铜,固体D中含有铜和过量的锌;
向D中加入稀硫酸时,铜不能和稀硫酸反应,锌和稀硫酸反应生成硫酸锌和氢气.
解答 解:(1)金属具有导电性,可以用作导线,具有导热性,可以用于制成炊具,铝具有延展性,可以制成铝箔,故选:B;
(2)Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,反应中Fe元素的化合价降低,则Fe2O3被还原,为氧化剂,硫酸铜和铁反应生成硫酸亚铁和铜,化学方程式为:Fe+CuSO4=FeSO4+Cu,156gAl(OH)3中含有铝元素的质量为:156g×$\frac{27}{78}$×100%=54g;
(3)①过程Ⅱ中分离操作的名称是过滤,可以把铜、锌和硫酸锌溶液分离;
②过程Ⅲ中有气体产生,是因为过量的锌和稀硫酸反应生成了氢气,反应的化学方程式为:Zn+H2SO4=ZnSO4+H2↑;
③溶液A中含有硫酸铜和硫酸锌,因此含有铜、锌两种元素;
固体C中含有铜和锌,因此含有铜、锌两种元素,故选:AC.
故答案为:(1)B;
(2)Fe2O3,Fe+CuSO4=FeSO4+Cu,54g;
(3)①过滤;
②Zn+H2SO4=ZnSO4+H2↑;
③AC.
点评 实验是化学的重要组成部分,正确的实验操作是得出科学结论的前提条件之一,因此要学会设计实验、进行实验、分析实验,为得出正确的结论奠定基础.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
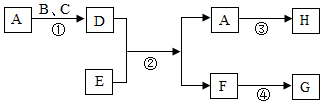 A-H是初中化学常见物质,其中D、H为红色固体,E为有毒气体,它们之间的转化关系如图所示,回答下列问题:
A-H是初中化学常见物质,其中D、H为红色固体,E为有毒气体,它们之间的转化关系如图所示,回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
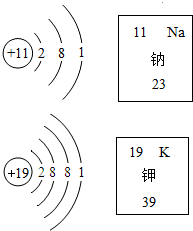 如图分别是钠和钾两种原子的结构示意图和它们在元素周期表中的部分信息.
如图分别是钠和钾两种原子的结构示意图和它们在元素周期表中的部分信息.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ②①③ | B. | ②③① | C. | ③②① | D. | ③①② |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 铁丝和铜丝分别插入稀硫酸中 | |
| B. | 铜丝插入硫酸亚铁溶液中 | |
| C. | 铁丝和铜丝分别在氧气中点燃 | |
| D. | 铁丝和铜丝分别插入氢氧化钠溶液中 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com