
 某班同学完成制取二氧化碳的实验后,对回收的盐酸和氯化钙混合溶液(不考虑其他杂质)进行了以下实验:取40mL该溶液于烧杯中,滴入40g溶质质量分数为13.8%的K2CO3溶液.滴入K2CO3溶液质量与生成沉淀质量的关系如图所示.求:
某班同学完成制取二氧化碳的实验后,对回收的盐酸和氯化钙混合溶液(不考虑其他杂质)进行了以下实验:取40mL该溶液于烧杯中,滴入40g溶质质量分数为13.8%的K2CO3溶液.滴入K2CO3溶液质量与生成沉淀质量的关系如图所示.求:分析 根据盐酸和氯化钙与碳酸钾反应的化学方程式就可计算出溶液中HCl;
当加入K2CO3的质量为30g时,所得溶液中溶质为氯化钾,根据氯化钙与碳酸钾反应的化学方程式和生成沉淀的质量,列出比例式,就可计算出生成KCl的质量,然后作出解答即可;
由图示数据可知,与盐酸反应的碳酸钾溶液的质量为10g,根据盐酸与碳酸钾反应的化学方程式,列出比例式,就可计算出盐酸与碳酸钾反应生成KCl的质量和溶液中HCl的质量;实验结束后,若将烧杯中的滤液蒸干,得到固体物质质量=生成KCl的质量+剩余K2CO3质量.
解答 解:从图象中的数据可以看出,10g之前没有出现沉淀,所以和盐酸反应的碳酸钾溶液是10g,从加入10g碳酸钾溶液开始出现沉淀,到30g后沉淀不变,说明和氯化钙反应的碳酸钾溶液是20g,生成沉淀是2g,
10g碳酸钾溶液中含有碳酸钾的质量为10g×13.8%=1.38g
设和碳酸钾反应的盐酸是x,生成氯化钾为y,生成二氧化碳的质量为z
K2CO3+2HCl═2KCl+H2O+CO2↑
138 73 149 44
1.38g x y z
$\frac{138}{1.38g}=\frac{73}{x}$=$\frac{149}{y}$=$\frac{44}{z}$
x=0.73g y=1.49g,z=0.44g
与氯化钙反应的碳酸钾的质量为:20g×13.8%=2.76g
设碳酸钙和碳酸钾反应生成氯化钾为b,
K2CO3+CaCl2═2KCl+CaCO3↓
138 149
2.76g b
$\frac{138}{2.76g}=\frac{149}{b}$
b=2.98g
反应后烧杯中的物质包括两个反应中生成的氯化钾,以及反应剩余的碳酸钾的质量,故:1.49g+2.98g+(40g-30g)×13.8%=5.85g.
答案:
(1)5.85g;
(2)所取40mL溶液中含HCl的质量为.73g;
点评 在解此类题时,首先根据图象分析反应的原理,然后再根据题中的条件利用方程式进行求解.最后的固体求酸注意要包含碳酸钙,因为题干要求的是烧杯内的物质.


 阶梯计算系列答案
阶梯计算系列答案科目:初中化学 来源: 题型:选择题
| A. | ②④⑥ | B. | ①④⑤ | C. | ④⑤⑥ | D. | ①③④ |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
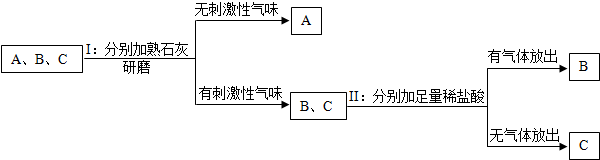
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 水能、风能、核能都是可再生能源 | |
| B. | 光纤通讯是依靠超声波来传递信息的 | |
| C. | 在通常情况下,铜、碳棒和陶瓷都属于导体 | |
| D. | 棉花属于天然有机材料 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 电解水实验说明水由氢、氧两种元素组成 | |
| B. | NaOH溶于水实验说明化学反应在生成新物质的同时还放出热量 | |
| C. | 用黄铜片在铜片上刻划实验说明合金一般比纯金属硬度大 | |
| D. | 稀释浓硫酸时将浓硫酸倒入水中是为了防止液滴四处飞溅 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
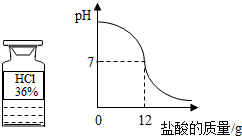 某同学在实验室看到一瓶久置的盐酸,为测定其试剂的溶质质量分数,在烧杯中加入20g溶质质量分数为20%的氢氧化钠溶液,逐滴加入该盐酸,pH测定仪记录了加入盐酸的质量与烧杯中溶液的pH关系(如图所示).
某同学在实验室看到一瓶久置的盐酸,为测定其试剂的溶质质量分数,在烧杯中加入20g溶质质量分数为20%的氢氧化钠溶液,逐滴加入该盐酸,pH测定仪记录了加入盐酸的质量与烧杯中溶液的pH关系(如图所示).查看答案和解析>>
科目:初中化学 来源: 题型:解答题
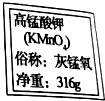 某同学准备用高锰酸钾制取氧气,他取出没开封的高锰酸钾试剂.看到瓶上标签如图所示.
某同学准备用高锰酸钾制取氧气,他取出没开封的高锰酸钾试剂.看到瓶上标签如图所示.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com