
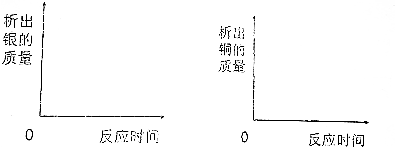
分析 根据在金属活动性顺序中,位置在前的金属能将位于其后的金属从其盐溶液中置换出来,铁>铜>银,铁能与硝酸铜反应生成硝酸亚铁和铜,能与硝酸银反应生成硝酸亚铁和银,生成的铜能与硝酸银反应生成硝酸铜和银进行分析.
解答 解:在金属活动性顺序中,位置在前的金属能将位于其后的金属从其盐溶液中置换出来,铁>铜>银,铁能与硝酸铜反应生成硝酸亚铁和铜,能与硝酸银反应生成硝酸亚铁和银,生成的铜能与硝酸银反应生成硝酸铜和银,逐渐加入一定质量的铁粉,若完全反应后溶液中溶质为3种,说明溶液中的溶质是硝酸铜、硝酸银、硝酸亚铁,硝酸银中的银没有被完全置换出来,所以溶液下方存在的金属单质为银,每56份质量的铁会生成216份质量的银,所以溶液质量的变化情况为溶液质量逐渐减小,铁和硝酸铜反应生成硝酸亚铁和铜,溶液质量减轻,化学方程式为:Fe+2AgNO3=Fe(NO3)2+2Ag,Fe+Cu(NO3)2=Fe(NO3)2+Cu.
故答案为:
硝酸银,Fe+2AgNO3=Fe(NO3)2+2Ag,硝酸铜,Fe+Cu(NO3)2=Fe(NO3)2+Cu,
点评 本题考查了金属活动性顺序的应用,完成此题,可以依据金属活动性顺序及其意义进行,注意金属在与两种金属的盐溶液发生置换反应时,会先置换活动性较弱的金属.


 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | H2SO4 Na2O C CO | B. | Mg(OH)2 CuSO4 C CO2 | ||
| C. | KOH HNO3 O2 SO3 | D. | HCl NaOH O2 P2O5 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验步骤 | 实验现象 | 实验结论 |
| ①取少量样品于试管中,加入 氯化钙溶液 | 生成白色沉淀 | 溶液只有部分变质 |
| ②取少量充分反应后的溶液与试管中,滴入 无色酚酞试液 | 溶液变红色 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
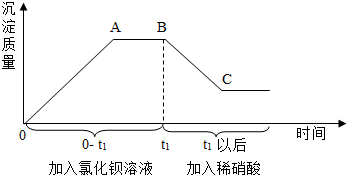
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 化学与人类生活的关系越来越切
化学与人类生活的关系越来越切 ,碘原子在化学反应中易形成$\underset{碘离子}{…}$I-.
,碘原子在化学反应中易形成$\underset{碘离子}{…}$I-.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com