
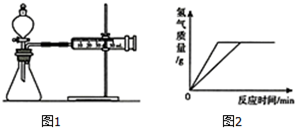
 某化学学习小组为比较镁和铁的金属活动性强弱设计了如下实验方案.
某化学学习小组为比较镁和铁的金属活动性强弱设计了如下实验方案.分析 【实验准备】(1)根据配置溶液的操作分析用到的仪器,根据稀释浓硫酸的要求及注意的事项分析;
(2)根据影响反应速率的因素分析需要控制的变量;
【探究一】根据金属与酸反应的剧烈程度比较金属的活泼性;
【探究二】
(1)根据检查装置气密性的原理分析;
(2)根据镁与硫酸的反应,写出反应的方程式;
(3)当金属过量时,与酸反应生成氢气的质量决定于酸的质量;
(4)据图象可以得出:a、比较氢气的多少,从而可以判断出金属的相对原子质量的大小,得到氢气多的则相对原子质量小;b、判断金属的活动性强弱,反应时间短或斜线斜率大的则该金属的活动性强
【探究三】本题可根据金属活动顺序及物质的化学性质,采用逐一验证法进行解答,也可正向理论推断;首先“向滤 出的固体中滴加稀硫酸,没有气泡产生“,说明固体中没有铁或镁;其次从金属活动顺序及题中给的信息“一定量的镁粉”进行判断.
解答 解:【实验准备】(1)用98%的浓硫酸配制l0%的硫酸溶液.除了需要上述仪器外,还 需要用到量筒量取浓硫酸以及水的体积,;在稀释浓硫酸时,一定要把浓硫酸慢慢注入水中,并不断搅拌,且不可将水倒入浓硫酸中;
(2)由于金属体积的大小影响与酸反应的速率.所以,要求两种金属片表面积相同的原因是控制变量;
【探究一】由于镁比铝的活动性强,所以,与硫酸反应时镁比铝反应更剧烈;
【探究二】
(1)如果装置不漏气,针筒的活塞被拉出一段后,针筒内压强变小,在大气压的作用下,活塞一段时间后又回到原来的位置;
(2)镁与硫酸反应生成了硫酸镁和氢气,反应的化学方程式是:Mg+H2S04═MgS04十H2↑;要比较两种金属活动性强弱,可以测定两种金属与硫酸反应得到相同体积氢气所需要的时间;还可测定相同时间内产生的气体体积;
(3)若镁和铁均过量,则装置甲中产生的H2的质量等于装置乙中产生的H2质量.
(4)A、由于铁的相对原子质量大,因此得到相同质量的氢气,参加反应的铁的质量要多一些,故A错误;
B、等质量的不同金属得到的氢气一样多,说明参与反应的金属的质量一定不一样多,因此至少有一种金属剩余,故B错误;
C、金属与酸反应,由于放入的金属的质量比产生的氢气的质量大,所以溶液的质量一定增大,故C正确;
D、由于得到的氢气一样多,根据元素的质量守恒可知,参加反应的稀盐酸和稀硫酸的溶质中氢元素的质量一定相等,从而说明参与反应的两种酸的质量一定不一样多,没说酸的量,所以可能都剩下,也可能一种剩余,故D错误;
故选C.
【探究三】根据金属活动顺序表知镁比铁活泼,铁比铜活泼,所以加入镁粉,首先镁粉和硫酸铜溶液反应,置换出单质铜,如果镁粉足量可以再继续和硫酸亚铁反应置换出铁,向滤出的固体中滴加稀硫酸,没有气泡产生,说明固体中不含有和稀硫酸反应的金属.
A、因为镁和硫酸铜、硫酸亚铁都能发生置换反应,所以滤出的固体中一定含有铜,故A正确;
B、因为“向滤 出的固体中滴加稀硫酸,没有气泡产生“,说明滤出的固体一定不含有铁或镁,故B错误;
C、因为“加入一定量的镁粉”,如果镁粉不足,则滤液中可能含有硫酸铜,故C正确;
D、由于,首先镁粉参与反应,所以滤液中一定有硫酸镁,固体中无铁,说明硫酸亚铁未反应,所以滤液中也一定有硫酸亚铁,故D正确;
故选:ACD.
故答为:(【实验准备】(1)量筒 把浓硫酸慢慢注入水中 (2)控制变量;
【探究一】镁比铝的金属活动性强;
【探究二】(1)不漏气; (2)Mg+H2S04═MgS04十H2↑,相同时间内产生的气体体积;(3)相等;(4)C.
【探究三】
【探究三】ACD.
点评 本题是一道综合知识题目,考查的角度较广,难度较大,要求学生具有分析和解决问题的能力.


科目:初中化学 来源: 题型:解答题

| 步骤 | 实验操作 | 实验现象 |
| ① | 将寒痛乐打开,将药物倒入一烧杯中,观察 | 药物为黑色固体粉末 |
| ② | 用一条形磁铁与烧杯中的黑色粉末充分接触,取适量吸附在磁铁上的黑色粉末放于燃烧匙中,在酒精灯上点燃后伸入盛有氧气的集气瓶中,观察 | 剧烈燃烧火星四射,放出热量,生成黑色固体 |
| 步骤 | 实验操作 | 主要实验现象 | 实验结论及解释 |
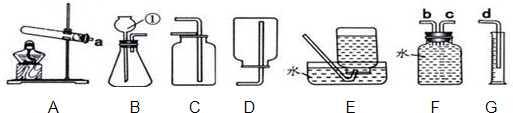
| ① | 连接好装置如上图所示,然后用手捂住集气瓶外壁. | 量筒导管口有气泡. | 装置的气密性良好 |
| ② | 加入足量药品,迅速将胶塞盖严,并充分振荡 | 放热,导管口有气泡冒出 一段时间后,量筒中的水沿导管逐渐被吸入到集气瓶中 | 进入集气瓶内水的体积即为空气中氧气的含量. |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 氯化钠可以用做工业除雪剂 | |
| B. | 人的胃液里含有少量的盐酸,可以帮助消化 | |
| C. | 50mL水和50mL酒精混合后,得到l00mL酒精溶液 | |
| D. | 用熟石灰可以改良酸性土壤 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | 品尝:白醋和糖水 | B. | 肥皂水:硬水和软水 | ||
| C. | 二氧化锰:水和过氧化氢溶液 | D. | 带火星的木条:氮气和二氧化碳 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com