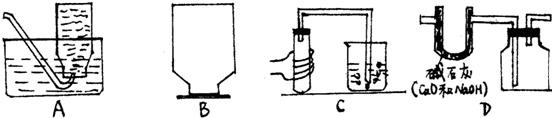
解:(1)根据仪器的图形和用途可知两仪器分别是酒精灯和试管;
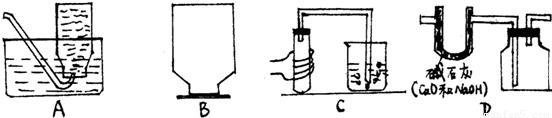
(2)氯酸钾制取氧气需要加热,属于“固体加热型”,故选发生装置A;氧气的密度比空气大且不易溶于水,所以可用向上排空气法或排水法收集;装药品之前应先检查装置的气密性,防止漏气;氯酸钾在加热和二氧化锰作催化剂的条件下生成氯化钾和氧气,方程式是2 KClO
3 
2KCl+3O
2↑;
(3)实验室制取二氧化碳用石灰石或大理石和稀盐酸,不需加热,属于“固液常温型”,应选择B作为气体发生装置,二氧化碳溶于水,密度比空气大,应采用D(向上排空气法)收集;
石灰石与稀盐酸反应生成氯化钙、水和二氧化碳,方程式是CaCO
3+2HCl=CaCl
2+CO
2↑+H
2O;根据B装置的特点可知,该装置不易控制反应速率,一旦混合不好终止反应,所以浪费药品;
故答案为:
(1)酒精灯、试管;
(2)A;C或D;检查装置气密性; 2KClO
3 
2KCl+3O
2↑;
(3)石灰石; 稀盐酸; B; D; CaCO
3+2HCl=CaCl
2+CO
2↑+H
2O.
不易控制化学反应速度或浪费药品等(合理答案均可)
分析:(1)根据仪器的图形和用途填写名称;
(2)根据氯酸钾制取氧气的反应条件及反应物判断发生装置;并由氧气的密度和溶解性确定收集装置;装药品之前应先检查装置的气密性,防止漏气,依据其反应原理书写方程式;
(3)实验室制取二氧化碳用石灰石或大理石和稀盐酸,不需加热,属于“固液常温型”,再依据二氧化碳的性质选择收集装置、依据反应原理书写方程式;根据B装置的特点可知,该装置不易控制反应速率,一旦混合不好终止反应.
点评:本题主要考查了装置的选取、反应方程式的书写及对仪器的认识等知识,了解相关知识才能正确解答;这是初中化学的重要考点,要认真掌握才能灵活应用.

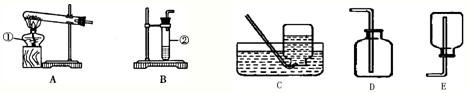
 2KCl+3O2↑;
2KCl+3O2↑; 2KCl+3O2↑;
2KCl+3O2↑;

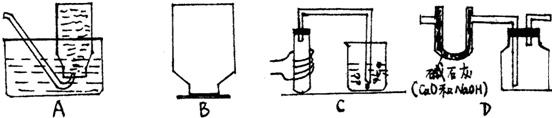
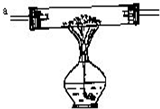 有两种黑色粉末A、B和两种无色气体C、D,用下面的装置图所示的装置做了以下实验:
有两种黑色粉末A、B和两种无色气体C、D,用下面的装置图所示的装置做了以下实验: